Подагра бестофусная форма что это
– Бестофусная формахарактеризуется отсутствием тофусов различных локализаций (подкожных, внутрикостных и других)
– Тофусная формасопровождается наличием тофусов различных локализаций ( подкожных, и/или внутрикостных, и других)
Предполагаемая формулировка диагноза
Течение подагры. Вариант артрита (при его наличии) или межприступный период при отсутствии артрита. Форма.
Например:
1. Подагра, рецидивирующее течение, бестофусная форма. Острый артрит.
2. Подагра, рецидивирующее течение, тофусная форма. Межприступный период.
3. Подагра, рецидивирующее течение, тофусная форма. Затяжной артрит. Нефролитиаз.
4. Подагра, хроническое течение, бестофусная форма. Межприступный период.
5. Подагра, хроническое течение, тофусная форма. Хронический артрит. Подагрическая нефропатия. Хроническая болезнь почек Ш ст.
Общие принципы фармакотерапии
Эффективность лечения во многом зависит от информированности пациентов о том, что для купирования острого приступа и лечения хронической подагры используются разные по механизму действия лекарственные средства.
Цели лечения:
· быстрое и безопасное купирование острого подагрического артрита;
· предупреждение рецидивов;
· предотвращение перехода болезни в хроническую стадию, сопровождающуюся образованием тофусов, поражением почек, деструкцией суставов.
ЛЕЧЕНИЕ ОСТРОГО ПРИСТУПА
Для лечения острого приступа подагры используют НПВП, ГКС (локально и системно), колхицин.
НПВП применяются в полных терапевтических дозах. Согласно рекомендациям института ревматологии РАМН препаратом выбора для купирования острого подагрического артрита является нимесулид по 100 мг от 2 до 4 раз в сутки. Кроме того, может назначаться диклофенак 200 – 400 мг/сут.
Колхицин,одно из древнейших средств для купирования острого подагрического артрита, в настоящее время в России не применяется. Это обусловлено медленным развитием лечебного эффекта и высокой частотой осложнений (диарея, миелосупрессия, почечная и сердечная недостаточность, ДВС синдром, гипокальциемия, судороги).
ГКС назначаются при невозможности использования НПВП из-за непереносимости препаратов или наличия почечной недостаточности и язвенного поражения ЖКТ.
Наиболее эффективно введение ГКС внутрисуставно с предварительным промыванием сустава. В мелкие суставы вводится 5–20 мг, в средние (локтевой, лучезапястный) – 10- 40 мг, в крупные суставы (коленный, голеностопный, плечевой) – 40 – 80 мг препарата.
В последние годы все чаще используются ГКС системного действия для купирования острого приступа.
Наиболее эффективно назначение метилпреднизолона в виде пульс – терапии. В первый день внутривенно капельно вводится 500 (или 250) мг препарата, во 2 и 3 день – по 250 мг.
Возможно также назначение триамцинолон ацетонида в/м 40 мг, при необходимости повторное введение через 24 ч или преднизолона внутрь 0,5 мг/кг в первые сутки, с последующим снижением дозы по 5 мг в каждые последующие сутки;
Из методов физиотерапии для купирования приступа применяются ультрафиолетовое облучение крови, электрическое поле УВЧ, импульсные токи по методике электросна.
ЛЕЧЕНИЕ ХРОНИЧЕСКОЙ ПОДАГРЫ
Безусловными показаниями для начала патогенетической, т. е. собственно противоподагрической терапии, направленной на нормализацию уровня мочевой кислоты, являются частые (3-4 раза в год) приступы острого подагрического артрита, хроническая подагра и нефролитиаз.
Она основана на комбинации немедикаментозных (снижение массы тела, диета, отказ от приема алкоголя, диуретической терапии) и медикаментозных методов лечения (антигиперурикемического лекарственного средства – аллопуринола и в ряде случаев урикозурических лекарственных средств).
Диетические рекомендации заключаются:
· в ограничении мясных и рыбных продуктов, бобовых, копченостей и консервов, острых приправ, специй (кроме уксуса и лаврового листа), некоторых овощей (шпинат, щавель, сельдерей, цветная капуста, редис), шоколада, крепкого кофе и чая, спиртных напитков (особенно пива и вина);
· в соблюдении режима питания (дробно, до 5 раз в сутки); 1 раз в неделю– разгрузочный день с употреблением овощей, фруктов (особенно, цитрусовых), молочных продуктов;
· в некотором увеличении объема выпиваемой жидкости (до 2-3 литров в день)
Кроме того, рекомендуется регулярное посещение бани или сауны, что способствует внепочечному выведению мочевой кислоты, контроль за подержанием нормальной массы тела и артериальным давлением (в лечении артериальной гипертензии, по возможности, не должны использоваться диуретики, особенно тиазидового ряда).
Терапию лекарственными препаратами следует начинать только после полного купирования приступа острого артрита и для профилактики обострений в течение первых нескольких месяцев после окончания приступа её необходимо сочетать с приемом небольших доз колхицина или НПВП.
При первичной подагре противоподагрические средства обычно назначаются для пожизненного ежедневного приема, их отмена приводит к быстрому (в течение 1- 3 недель) повышению уровня мочевой кислоты в крови и возобновлению клинических проявлений.
АЛЛОПУРИНОЛ – ингибитор ксантиноксидазы, подавляет синтез мочевой кислоты, являясь эффективным средством как при её гиперпродукции, так и при её гипоэкскреции. Он абсолютно показан при стойком увеличении уровня мочевой кислоты более 0,6 ммоль/л, а также, в отличие от урикозурических средств, при почечной недостаточности, нефролитиазе, гиперурикозурии. На фоне лечения аллопуринолом сывороточный уровень мочевой кислоты начинает снижаться уже в течение первых 2 дней, стабильный максимальный эффект развивается через 2 недели.
Нельзя начинать антигиперурикемическую терапию во время острой атаки артрита – необходимо вначале максимально купировать воспалительные явления в суставах. Если приступ развился на фоне приема антигиперурикемических препаратов, лечение необходимо продолжить с дополнительным назначением адекватной противовоспалительной терапии.
Целевой уровень мочевой кислоты крови – 360 мкмоль/л.
Для того чтобы избежать резкого снижения уровня мочевой кислоты, которое может спровоцировать острый приступ подагры, лечение следует начинать с небольшой дозы аллопуринола – 50–100 мг/сут с титрованием до нормоурикемии.
Отражением правильного выбора дозы препарата является скорость снижения уровня гиперурикемии – не более 0,04 мкмоль/л или 10% от исходного значения в течение одного месяца терапии. По мнению многих авторов, правилен подход: «чем медленнее, тем лучше». На фоне проводимой терапии необходим мониторинг уровня азотемии: 1 раз в 3 недели в начале терапии и каждые 6 недель в последующем.
Обычная доза аллопуринола — 200–300 мг/сут., при необходимости — 600 мг/сут. и более. Пожилым пациентам со сниженной клубочковой фильтрацией (менее 50 мл/мин), с очень частыми атаками артрита следует назначать аллопуринол в дозе не более 100 мг/сут. При подборе дозы следует учитывать скорость клубочковой фильтрации: при скорости менее 30 мл/мин обычно назначаются низкие дозы препарата.
Рассасывание подкожных тофусов наблюдается не ранее чем через 6-12 месяцев непрерывной терапии аллопуринолом.
Источник
Бестофусная формахарактеризуется отсутствием тофусов различных локализаций (подкожных, внутрикостных и других).
Тофусная формасопровождается наличием тофусов различных локализаций (подкожных, и/или внутрикостных, и других).
Примеры формулировки диагноза
Течение. Вариант артрита (при его наличии) или межприступный период при отсутствии артрита. Форма.
1. Рецидивирующее течение. Острый артрит. Бестофусная форма.
2. Рецидивирующее течение. Межприступный период. Тофусная форма.
3. Рецидивирующее течение. Затяжной артрит. Тофусная форма. Нефролитиаз.
4. Хроническое течение. Межприступный период. Бестофусная форма.
5. Хроническое течение. Хронический артрит. Тофусная форма. Подагрическая нефропатия. Хроническая болезнь почек III ст.
Необходимо помнить, что подагра – это тофусная болезнь, поражающая любой внутренний орган.
Диагностика
В 1999 г. экспертами ВОЗ были рекомендованы классификационные критерии диагноза подагры(S.L. Wallace et al., 1977):
1. Наличие характерных кристаллов моноурата натрия в синовиальной жидкости (абсолютный критерий).
2. Наличие тофусов, содержание кристаллов моноурата натрия в которых подтверждено химически или поляризационной микроскопией(абсолютный критерий).
3. Наличие любых 6 из 12 ниже перечисленных признаков:
• более одной атаки острого артрита в анамнезе;
• максимальное развитие воспаления сустава в первый день болезни;
• моноартрит;
• гиперемия кожи над пораженным суставом;
• боль и воспаление в первом плюснефаланговом суставе;
• асимметричное поражение первого плюснефалангового сустава;
• одностороннее поражение суставов стопы;
• подозрение на тофусы;
• гиперурикемия;
• асимметричный отек суставов;
• субкортикальные кисты без эрозий при рентгенографическом исследовании;
• отрицательные результаты при посеве синовиальной жидкости.
В синовиальной жидкости в период острого приступа подагрического артрита выявляется увеличение количества лейкоцитов до 10 000 – 20 000 клеток/мм3, преимущественно нейтрофилов.
Наиболее важный метод диагностики подагры – поляризационная микроскопия синовиальной жидкости и других тканей (например, тофусов), позволяющая обнаружить кристаллы уратов, размерами 3 – 30 мкм, характерной иглообразной формы и оптическим свойством – отрицательным двойным преломлением луча. Кристаллы моноурата натрия образуются только при подагре, поэтому являются абсолютным диагностическим критерием.
Определение сывороточного уровня уратов в период острой подагрической атаки имеет ограниченное диагностическое значение, так как в это время отмечается, с одной стороны, повышенное выведение мочевой кислоты почками, с другой – мочевая кислота максимально концентрируется в воспаленных суставах и снижается ее содержание в сыворотке крови. В различные периоды этот уровень, как правило, повышен у подавляющего большинства больных, однако нормальный уровень уратов не исключает диагноз подагры.
Определение суточной экскреции мочевой кислоты имеет диагностическое значение лишь у молодых пациентов с нормальной функцией почек, у которых повышение содержания мочевой кислоты в моче говорит о гиперпродукции мочевой кислоты. При снижении функции почек, у пожилых больных нормальный или даже пониженный уровень экскреции мочевой кислоты может быть и при выраженной гиперпродукции мочевой кислоты. Рентгенологическая диагностика основана на выявлении типичных внутрикостных кистовидных образований различных размеров с четкими контурами, краевых эрозий. Эти изменения связаны с внутрикостным отложением кристаллов моноурата натрия (тофусы). На поздних стадиях заболевания развивается деструкция не только хряща и субхондральной кости, но и всего эпифиза и даже части диафиза с наиболее выраженными поражениями суставов стоп и кистей.
Целевой уровень мочевой кислоты крови у больных подагрой – менее 360 мкмоль/л (как у мужчин, так и у женщин).
Чрезвычайно актуальной проблемой у пациентов, страдающих подагрой, является возникновение артериальной гипертензии.
Возможные механизмы повышения артериального давления
При гиперурикемии
Предполагают, что существует несколько потенциальных механизмов, благодаря которым уровень мочевой кислоты может играть патогенетическую роль в развитии сердечно-сосудистой заболеваемости или, наоборот, воздействовать на клинические проявления у пациентов с установленным атеросклерозом.
В эксперименте было показано, что высокий уровень мочевой кислоты может индуцировать сосудистое повреждение, прекращавшееся при использовании аллопуринола. Также известно, что гиперурикемия вызывает констрикцию почечных сосудов, коррелирует с активностью РАС, участвует в развитии дисфункции эндотелия. Имеются данные о том, что мочевая кислота индуцирует пролиферацию сосудистых гладкомышечных клеток in vitro, активируя факторы транскрипции и сигнальные молекулы, вызывая гиперэкспрессию циклооксигеназы, тромбоцитарного фактора роста и моноцитарного хемоаттрактантного белка. Мочевая кислота и фермент ксантиноксидаза часто выявляются в атеросклеротических бляшках. Свободные радикалы, встречающиеся при гиперурикемии различного генеза, стимулируют перекисное окисление липидов, ответственное за утолщение комплекса интима–медиа сонных артерий. Другие потенциальные механизмы, с помощью которых гиперурикемия и/или повышенная активность ксантиноксидазы могут способствовать сосудистому повреждению, включают адгезию тромбоцитов, пролиферацию гладкомышечных клеток сосудов и стимуляцию воспалительного ответа. Это позволило предположить, что гиперурикемия повышает риск коронарного тромбоза у пациентов с уже имеющимися коронарными заболеваниями.
Таким образом, гиперурикемия является независимым фактором риска сердечно-сосудистых заболеваний, поэтому диагностика и лечение подагры, гиперурикемии, осложнений заболевания является актуальной проблемой терапии.
Источник
У пациентов пожилого и старческого возраста, как правило, наблюдается атипичное начало острой подагры. Наиболее часто дебют подагрического артрита у данной группы пациентов характеризуется менее выраженным болевым синдромом и поражением не одного, а нескольких суставов (Таблица 29) (Арьев А.Л., 2012).
Таблица 29. Сравнительная характеристика клинических проявлений острого подагрического артрита у пациентов в зависимости от возраста (Арьев А.Л., 2012)
| Классические проявления подагры (подавляющее большинство пациентов среднего возраста) | Атипичные проявления подагры (у пожилых пациентов) |
Поражение одного сустава (моноартрит) | Поражение нескольких суставов (полиартрит) |
Внезапное начало (острый приступ артрита) | Постепенное начало (медленное) |
< 10% у женщин | Соотношение мужчин и женщин одинаковое |
Этиологические причины различны | Изменение почечной функции |
Кристаллы моноурата натрия, первичное поражение 1 плюснефалангового сустава стопы | Возможно наличие кристаллов пирофосфата кальция с формированием псевдоподагры, первичное поражение коленных, лучезапястных, плечевых и голеностопных суставов |
Некоторыми исследователями отмечено, что у пациентов пожилого возраста также часто наблюдается и развитие псевдоподагры, характеризующейся более медленным течением, с поражением в начале заболевания коленных, лучезапястных, плечевых или голеностопных суставов. Учитывая возможное сочетание этих заболеваний в пожилом возрасте, а также наличие дегенеративно-дистрофических изменений в суставах, необходимо проводить тщательную дифференциальную диагностику у каждого пациента пожилого возраста.
Использование некоторых лекарственных препаратов, таких как мочегонные препараты и ацетилсалициловая кислота, у пациентов пожилого возраста может приводить к развитию или усилению подагры, однако они необходимы для лечения многочисленной сопутствующей патологии, имеющейся в этом возрасте. Необходимо использовать альтернативные механизмы, способствующие уменьшению уровня мочевой кислоты, в частности это касается диеты и потребления алкоголя (Арьев А.Л., 2012).
Первый приступ подагрического артрита у большинства пациентов может купироваться самостоятельно (Арьев А.Л., 2012). В то же время, наличие периода межприступной подагры дает важное клиническое преимущество, так как именно в этот период наиболее целесообразно и безопасно (в плане риска спровоцировать внеочередной приступ острого подагрического артрита) начинать собственно противоподагрическую терапию (Барскова В. Г., 2009).
Коварство этой болезни заключается еще и в том, что, несмотря на якобы светлые промежутки и кажущуюся благополучность, однажды начавшееся кристаллообразование постоянно продолжает развиваться в организме больного. Свидетельством этого является обнаружение многочисленных кристаллов моноурата натрия в различных органах и тканях, протекающее бессимптомно. Кристаллы урата натрия выявляются не только в суставах, пораженных по данным анализа болезни или на момент проведения микроскопического исследования, но и в тех суставах, где никогда ранее воспаление не наблюдалось (Селицкая О.В., Борисенко Н.А., 2009).
Хроническая тофусная подагра сопровождается развитием стойкого хронического артрита и формированием тофусов (часто множественных), поражения почек, мочекаменной болезни(Селицкая О.В., Борисенко Н.А., 2009) (Елисеев М.С., Хренников Я.Б., 2007).
Тофусы представляют собой депозитные отложения моноурата натрия. Хотя подкожные тофусы входят в число 12 основных клинических критериев подагры, они возникают уже на поздней стадии заболевания. В среднем же появления тофусов следует ожидать через 6–11 лет после первой атаки подагрического артрита, через 6 лет после дебюта заболевания подкожные тофусы выявляются уже у 40% больных, причем в ряде случаев они возникают после одного или нескольких приступов подагрического артрита. Часто при развитии кристаллиндуцированного воспалительного процесса или в результате дистрофических изменений кожных покровов на фоне локальной ишемии в области тофусов происходят прорыв их содержимого и формирование раневого дефекта. При значительном размере вскрывшегося тофуса могут возникать длительно незаживающие хронические язвы, причем одним из наиболее тяжелых осложнений считается их инфицирование (Елисеев М.С., Хренников Я.Б., 2007)
Тофусы могут локализоваться подкожно или внутрикожно в области пальцев кистей и стоп, коленных суставов, на локтях и ушных раковинах, но могут образовываться практически на любых участках тела и внутренних органах; у пожилых больных тофусы нередко располагаются в области узелков Гебердена. Иногда наблюдается изъязвление кожи над тофусами со спонтанным выделением содержимого в виде пастообразной белой массы. Обычные сроки появления тофусов – на 5-6-й год болезни.
Однако раннее появление тофусов также может наблюдаться, например, при некоторых формах ювенильной подагры, у женщин, принимающих диуретики, при некоторых заболеваниях почек, в частности хронической почечной недостаточности, сопровождающихся выраженной гиперурикемией. Тофусное поражение, как правило, сочетается с хроническим артритом и склонностью к полиартикулярному течению (Барскова В. Г., 2009). Рентгенологически выявляются солидные уратные отложения, в том числе в костной ткани. Тофусные поражения не болезненные, однако, при гистологическом исследовании отмечается хроническое гранулематозное воспаление и редко острое, напоминающее подагрический артрит в одном или нескольких тофусах (Селицкая О.В., Борисенко Н.А., 2009) (Рисунки).

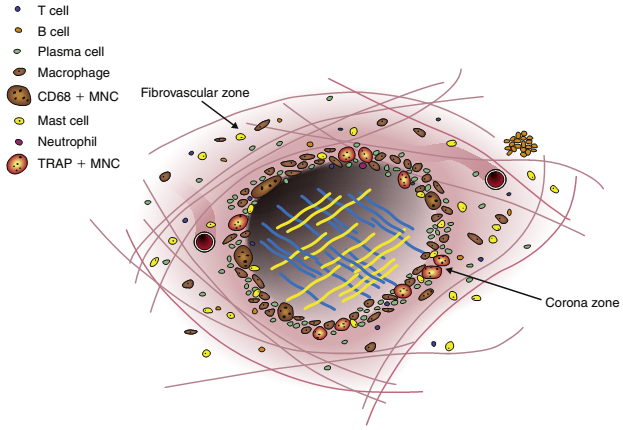
Рисунок 19. Клеточная модель подагрического тофуса (TerkeltaubR., 2012)
Примечание – кольцевая и фиброваскулярная зона тофуса представлены различными клеточными типами, определяемыми иммуногистохимическими методами. Эти зоны ограничивают участок, с локализованными в нем «упакованными» кристаллами мочевой кислоты, окружённых фагоцитами, тучными клетками, Т- и В-лимфоцитами, а также плазматическими клетками.
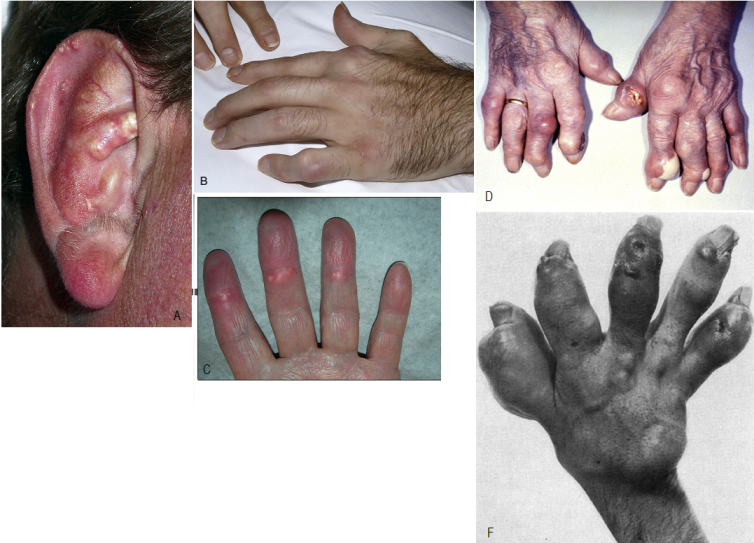
Рисунок 20. Клинические (суставные) проявления хронической тофусной подагры: «классические» тофусы на хряще ушной раковины (А), тофусы в проксимальных и дистальных межфаланговых суставах (В), нетипичные подкожные тофусы в дистальных межфаланговых суставах (С); тяжелая «злокачественная» тофусная подагра с ульцеративными тофусами на поверхности межфаланговых суставов (D, F) (Terkeltaub R., 2012) (Weisman M.H., 2010)
В настоящее время подагра известна не только и не столько как моно- илиполиартрит рецидивирующего и хронического течения, но и как серьезное системное заболевание. В клинической картине подагры наблюдаются поражения многих висцеральных органов, из них наиболее часто поражение почек– подагрическая нефропатия. Подагрическая нефропатия колеблется в широких пределах– от30% до75%. Развитие подагры связано собразованием тофусов в канальцах, уратных камней в лоханках почек, что способствует возникновению тубулоинтерстинального нефрита. Довольно часто и рано возникает мочекаменная болезнь.
Нередко у больных подагрой наблюдается артериальная гипертония. По данным ряда авторов артериальная гипертония диагностируется более чем у половины больных подагрой. В рамках одно исследования, в ходе которого наблюдались пациенты, не страдавшие подагрой, выявлена достоверная зависимость между гиперурикемией и развитием артериальной гипертонии. В дальнейших исследованиях было показано, что пациенты с уровнем мочевой кислоты выше300 мкмоль/лпредставляют собой особую группу, в которой риск развития поражения органов-мишеней усугубляется не только метаболическими расстройствами, нои нарушением суточного профиля АД. Эпидемиологические исследования подтверждают положительную связь между повышением уровня мочевой кислоты и риском развития коронарных заболеваний.
Рядом исследователей установлено, что ИБС у больных с подагрой встречается в 2-4 раза чаще, чем в целом в общей популяции соответствующего возраста. У больных подагрой выявляется ИБС и церебральный атеросклероз в 42-45% случаев. Причем атеросклероз отмечается в 2 раза чаще, нежели у лиц, не имеющих подагру в анамнезе. Существует мнение, что эти заболевания у больных подагрой развиваются не вследствие воздействия уратов на сосудистую стенку, а в результате сопутствующих подагре нарушений липидного обмена. Во многих исследованиях обнаружено, что уровень мочевой кислоты связан сгипертриглицеридемией. Так, повышение уровня триглицеридов отмечается в 50-70% случаев, агипертриглицеридемия в сочетании с гиперурикемией– в 82%. Результаты завершенных исследований свидетельствуют о том, что гиперурикемия является предиктором развития сердечно-сосудистых событий и смерти у больных с артериальной гипертензией, застойной СН, а также может рассматриваться как независимый фактор риска сердечно-сосудистых осложнений.
Проведенные исследования указывают на необходимость более раннего выявления висцеропатий, предупреждающих развитие коронарных и мозговых катастроф. Следовательно, необходимо раннее и детальное обследование сердечно-сосудистой и мочевыделительной систем у таких больных, проведение лечения с учетом имеющихся изменений (Селицкая О.В., Борисенко Н.А., 2009).
‹‹ Предыдущая Следующая ››
Автор материала: Булгакова Яна Сергеевна, кандидат биологических наук, ООО Сайнсфайлз
Также стоит почитать:
Медицинские центры, врачи
Опросы, голосования
Источник
