Лечение пневмонии у вич инфицированных детей
Пневмония у ВИЧ-инфицированных характеризуется особенностью возбудителей инфекции, течения заболевания и лечения. Нередко клиническая картина ничем не отличается от других видов воспаления лёгких, однако в виду отсутствия у врачей настороженности в отношении ВИЧ-инфекции, диагностика иммунодефицитных пневмоний затруднительна.

В Юсуповской больнице пульмонологи применяют современную аппаратуру и инновационные методы обследования, позволяющие быстро установить точный диагноз. Для лечения пациентов пульмонологи используют современные препараты, эффективно действующие в условиях иммунодефицита. В клинике терапии работают врачи, имеющие огромный опыт лечения иммунодефицитных пневмоний. Все сложные случаи воспаления лёгких обсуждаются на заседании экспертного Совета.
Причины пневмонии при ВИЧ-инфекции
Пневмонию у ВИЧ-инфицированных вызывают грамотрицательные палочки. Часто при наличии иммунодефицита в виде пневмонии протекает туберкулёз. Одними из наиболее известных и значимых возбудителей оппортунистических пневмоний у ВИЧ-инфицированных пациентов в эру ретровирусной терапии остаются пневмоцисты.
Развитие пневмоцистной пневмонии определяет не только степень выраженности иммунодефицита, но и его характер. Средняя частота пневмоцистной пневмонии при ВИЧ-инфекции в настоящее время составляет 50 %, а при других иммунодефицитных состояниях не превышает 1 %. Развитию воспаления лёгких способствует нарушение клеточного и гуморального иммунитета.
Клинико-диагностические критерии пневмонии
Диагностика пневмонии у ВИЧ-инфицированных является сложной из-за отсутствия патогномоничных клинических признаков, частого сочетанного течения нескольких оппортунистических заболеваний одновременно на фоне глубокого поражения иммунной системы. Отсутствуют и точные лабораторные критерии, которые позволяли бы подтвердить диагноз.
Пневмония у ВИЧ-инфицированных начинается подостро. На протяжении нескольких недель нарастают следующие симптомы:
- лихорадка;
- одышка;
- сухой кашель;
- чувство тяжести в грудной клетке;
- утомляемость;
- похудание.
Во время физикального исследования врачи обнаруживают лихорадку и учащённое дыхание, перкуссия и аускультация грудной клетки изменений не выявляют. В Юсуповской больнице пациентам с подозрением на иммунодефицитную пневмонию делают крупнокадровую флюорографию или рентгенографию в двух проекциях. На рентгенограммах можно увидеть двусторонние изменения – ограниченные затемнения легочных полей или сетчатую перестройку легочного рисунка. Иногда пульмонологи видят множественные очаговые тени или круглые полости. У некоторых ВИЧ-инфицированных больных изменений, характерных для воспаления лёгких, может совсем не быть. В этом случае в Юсуповской больнице пациентам делают компьютерную томографию.
Изменения лабораторных показателей неспецифичны. В большинстве случаев пневмоний у ВИЧ-инфицированных увеличивается активность лактатдегидрогеназы, однако это бывает и при других респираторных заболеваниях на фоне СПИДа. При измерении газового состава крови врачи иногда обнаруживают гипоксемию, увеличение парциального давления кислорода и респираторный алкалоз (смещение рН в кислую сторону). Характерным признаком инфекции является снижение парциального давления кислорода при физической нагрузке.
Поскольку пневмоцистную пневмонию легко спутать с другими свойственными ВИЧ-инфицированным заболеваниями, а курс лечения долгий и сопряжён с тяжелыми побочными эффектами, врачи Юсуповской больницы для подтверждения диагноза используют лабораторные методы. Сначала прибегают к иммунофлюоресцентному окрашиванию мокроты с использованием моноклональных антител. Если возбудитель не найден, выполняют диагностическую бронхоскопию и трансбронхиальную биопсию лёгкого. Если бронхоскопия оказалась неинформативной или состояние пациента ухудшается, врачи клиник-партнёров проводят открытую биопсию лёгкого.
Золотым стандартом диагностики пневмонии у ВИЧ-инфицированных является микроскопическая визуализация возбудителя. В настоящее время часто используют иммунофлюоресцентную диагностику с использованием моноклональных антител. Серологические методы могут быть малоинформативными из-за выраженного иммунодефицита. В клиниках-партнёрах проводят молекулярную диагностику иммунодефицитных пневмоний.
При исследовании периферической крови специфических изменений при пневмоцистной пневмонии не наблюдается. Диагностировать пневмоцистную пневмонию помогает высокий уровень скорости оседания эритроцитов. Часто имеют место изменения в крови, характерные для поздних стадий СПИДа.
Лечение пневмонии у ВИЧ-инфицированных
Основным препаратом для лечения пневмонии у ВИЧ-инфицированных пациентов является ко-тримоксазол (комбинация триметоприма и сульфаметоксазола). При недостаточной эффективности или непереносимости ко-тримоксазола пациентам в европейских странах назначают пентамидин для внутривенного введения. Данный препарат не зарегистрирован в РФ и врачи Юсуповской больницы его не применяют.
Резервной схемой лечения пневмоцистной пневмонии умеренной степени тяжести является комбинация клиндамицина с примахином. Схема лечения пневмонии у ВИЧ-инфицированных обязательно включает комбинированную антиретровирусную терапию, если пациент не получал её ранее. Кортикостероидные гормоны назначают на фоне начала антибактериальной терапии с целью предупреждения усиления дыхательной недостаточности.
Запишитесь на приём к пульмонологу по телефону клиники. Контакт-центр Юсуповской больницы работает круглосуточно. Пациентов с симптомами пневмонии в зависимости от тяжести течения заболевания госпитализируют в клинику терапии или отделение реанимации и интенсивной терапии. Пульмонологи лечат пациентов с воспалением лёгких согласно европейских рекомендаций, используют индивидуальные схемы терапии.
Источник
Пневмоцистная пневмония — редкая форма патологии легких, вызываемая внеклеточным грибом Pneumocistis jiroveci, поражающая лиц с тяжелыми дефектами иммунитета, больных, принимающих иммуносупрессивную терапию, онкологических больных, недоношенных и ослабленных детей, ВИЧинфицированных пациентов в стадии СПИДа. По таксономическому положению пневмоцисты относят к высшим грибам — аскомицетам или базидиомицетам, для них также характерны некоторые свойства протозоев [8]. Распространенность пневмоцист в природе широкая, выявляют пневмоцисты не только у людей, но и у животных. Для человека патогенна P. jiroveci, названная в честь чешского ученого-паразитолога Отто Йировеца, впервые описавшего этот микроорганизм как причину заболевания у человека.
Заражение происходит воздушно-капельным путем. Пневмоцисты обладают тропизмом к легочной паренхиме и не вызывают поражения верхних и средних дыхательных путей. Сезонность заболевания не характерна. Развитие пневмоцистоза определяется биологическими свойствами возбудителя и состоянием иммунной системы человека и связано с поражением как гуморального, так и клеточного иммунитета, в том числе с лимфоцитозависимым дефектом макрофагов, не распознающих размножающихся пневмоцист [3]. Клетками-мишенями для пневмоцист являются альвеолоциты 1-го типа, поражение которых проявляется деструкцией клеток, нарушением целостности альвеолярной мембраны и развитием экссудативных явлений. Для построения собственной клеточной оболочки P. jiroveci используют фосфолипиды сурфактанта человека. Это приводит к общему повреждению сурфактантного обмена: дисбалансу в уровнях сурфактантных фосфолипидов и протеинов, гиперсекреции сурфактанта [1]. Активность альвеолярных макрофагов при этом направлена на защиту альвеол от избыточной продукции сурфактанта, а не на поглощение возбудителя. Гиперпродукция сурфактанта на фоне развивающейся дисфункции альвеолярных макрофагов приводит к заполнению альвеол относительно гомогенной пенистой массой. Белки экссудата разрушают и инактивируют сурфактант, активируют фиброзирование межальвеолярных перегородок, что приводит к гипоксемии. Происходит снижение секреторной функции альвеолоцитов 2-го типа и возрастание их пролиферативной активности [7].
Частота пневмоцистной пневмонии у больных ВИЧ-инфекцией в странах Европы и США достигает 60%. Летальность от пневмоцистной пневмонии в среднем составляет 13%. В России частота пневмоцистной пневмонией у ВИЧ-инфицированных колеблется от 5,6 до 8,5%. Летальные исходы от пневмоцистной пневмонии у больных с поздними стадиями ВИЧ-инфекции составляют 7,1% и занимают 4 место после туберкулеза, бактериальной пневмонии, инфекционного эндокардита [4]. Заболевание, как правило, ограничивается легкими, но при глубокой иммуносупрессии возможны генерализованные формы. Пневмоцистная пневмония — наиболее частая СПИД-индикаторная патология у детей; ее частота у больных СПИДом детей, по данным центра по контролю заболеваний (CDC) США 1995 г., составляла 34% от всех случаев СПИДа у детей. Чаще эта инфекция развивается у детей первого года жизни (57—72% случаев), пик заболеваемости приходится на возраст 3—6 мес, поэтому детям первого года жизни особенно показана медикаментозная профилактика. Риск пневмоцистной пневмонии на первом году жизни у ВИЧинфицированных детей, не получающих профилактику, составляет 7—20%. Пневмоцистная пневмония может сочетаться с другими инфекционными поражениями легких на фоне ВИЧ-ассоциированной иммуносупрессии, что значительно усложняет диагностику. У детей, получающих профилактику бисептолом, пневмоцистная пневмония практически не регистрируется. Пневмоцистная пневмония — самая частая причина смерти младенцев, инфицированных ВИЧ, от нее умирают 50—60% младенцев на стадии СПИДа [6]. Диагностика пневмоцистной пневмонии сложна из-за отсутствия патогномоничных клинических признаков, частого сочетания с несколькими инфекционными заболеваниями на фоне глубокой депрессии иммунной системы, а также трудностей лабораторного подтверждения. Самым важным для диагностики пневмоцистной пневмонии является клиническая настороженность в отношении к этой инфекции у ВИЧ-инфицированных. В клинической картине пневмоцистной пневмонии у больных ВИЧ-инфекцией отмечается подострое начало заболевания, субфебрильная или небольшая фебрильная лихорадка, непродуктивный, навязчивый, приступообразный кашель, длящийся несколько недель или месяцев или постоянный, мучительный кашель, экспираторная или смешанная одышка, возникающая вначале при физической нагрузке, а затем и в покое, прогрессирующая дыхательная недостаточность. Может выделяться пенистая мокрота. Над легкими может определяться укорочение перкуторного звука, аускультативно жесткое дыхание, рассеянные сухие хрипы, крепитация, больше в задних отделах легких [2].
Рентгенологические изменения в легких характеризуются двусторонним прикорневым усилением сосудистого рисунка, снижением пневматизации, появлением «облаковидных» инфильтратов с обеих сторон, при прогрессировании процесса определяются множественные очаговые тени по типу «ватных» легких [5].
Подтверждение диагноза основано на выделении пневмоцист из бронхоальвеолярного лаважа или мокроты, «золотым стандартом» диагностики является микроскопическое обнаружение пневмоцист [5]. Экспресс-методом диагностики инфекции является полимеразная цепная реакция (ПЦР) с определением мРНК или ДНК пневмоцист в секрете бронхов [8]. Иммунофлюоресцентный метод диагностики имеет определенные погрешности и занимает больше времени.
Лечение пневмоцистной пневмонии на фоне ВИЧ-инфекции должно проводиться в сочетании комбинированной антиретровирусной терапии и предусматривает назначение котримоксазола в дозе 20 мг/кг по триметоприму. В тяжелых случаях для предупреждения развития дыхательной недостаточности применяют глюкокортикостероиды.
Представляем клиническое наблюдение поражения легких пневмоцистной этиологии у ребенка с ВИЧ-инфекцией.
Ребенок П., 4 мес (дата рождения 13.04.2015), переведен 02.09.2015 в ОРИТ № 2 ДИКБ № 6 из ИКБ № 1 в связи с ухудшением состояния с диагнозом «смешанная инфекция: РСВинфекция + острая герпетическая инфекция + острый хламидиоз, тяжелая форма. Бронхообструктивный синдром 2 степени. Носитель HCV-антигена. Незаконченный тест на ВИЧ». Из анамнеза известно, что ребенок от матери 29 лет, с отягощенным соматическим анамнезом (ВИЧ-инфекция с 2006 г., HCV+ с 2007 г., эктопия шейки матки), от 1-й беременности. Беременность протекала без особенностей. Роды первые срочные. Мальчик родился на сроке гестации 40 нед с длиной 53 см и массой тела 3350 г. Оценка по шкале Апгар 7/8 баллов. При рождении диагностирована родовая травма: линейный перелом правой теменной кости, кефалогематома правой теменной кости. Состояние ребенка было тяжелым за счет синдрома угнетения ЦНС, после рождения переведен в ОРИТ на самостоятельном дыхании. Мать скрыла факт ВИЧ-инфицированности, в связи с чем профилактическое лечение новорожденному антиретровирусными препаратами началось через 72 ч после родов. В возрасте 4 сут жизни ребенок переведен в ДИКБ № 6 в отделение для новорожденных детей от родителей с ВИЧ-инфекцией с диагнозом «врожденная пневмония. Церебральная ишемия 2 ст., синдром угнетения. Неонатальная желтуха. Перинатальный контакт по ВИЧ? HCV-носительство». За время нахождения в стационаре ребенок обследован по поводу перинатального контакта по ВИЧ-инфекции. Анализ крови на РНК HIVI методом ПЦР от 20.04.2015: не обнаружен. Иммуноблот от 22.04.2015: положительный. Получал курс профилактической АРВ-терапии (ретровир). 06.05.2015 был выписан домой в удовлетворительном состоянии с рекомендациями о продолжении курса ретровира с последующим обращением и постановкой на учет в МГЦ СПИД. Со слов матери, курс ретровира был проведен полностью (согласно рекомендациям в выписке из истории болезни). В МГЦ СПИД для постановки на учет и дообследование мама с ребенком не явилась. Находился дома; со слов матери, ребенок не болел. Впервые ребенок заболел 02.08.2015, когда появились симптомы кандидоза слизистых оболочек полости рта, получал лечение амбулаторно, на фоне проведенного лечения явления молочницы купированы. С 10.08.2015 отмечался подъем температуры тела до фебрильных цифр и сухой кашель, явления ринита. Получал симптоматическую терапию по назначению участкового педиатра. В динамике состояние с ухудшением, в связи с чем с клиникой обструктивного бронхита 24.08.2015 ребенок был госпитализирован в ИКБ № 1. При обследовании у ребенка были выявлены маркеры РСВ-инфекции, герпетической инфекции (I типа), хламидийной инфекции, получал комплексное лечение, однако состояние резко ухудшилось, и ребенок был переведен в ОРИТ ДИКБ № 6.
При поступлении в ОРИТ состояние ребенка крайне тяжелое за счет дыхательной недостаточности III степени, НК-II АB ст. ДВС-синдрома, проявлений инфекционного токсикоза, метаболических нарушений (метаболический и респираторный алкалоз) на фоне двусторонней полисегментарной пневмонии, язвенного энтероколита, манифестации ВИЧ-инфекции и развития иммунодефицитного состояния. Сатурация кислорода при поступлении — 65%. В экстренном порядке проведены интубация трахеи с переводом на ИВЛ и мероприятия, направленные на обеспечение центрального венозного доступа (катетеризация правой подключичной вены 02.09.2015), начата интенсивная терапия. С момента поступления ребенок находился на жестких параметрах ИВЛ в режиме гипервентиляции, ЧД 50—52, T вд. 0,47—0,60 с, PееP 5—6 мбар, PIP 23—25 мбар, FiO2 90—85—80%. Длительно, более одной недели, сохранялась выраженная кислородозависимость от высоких концентраций кислорода при проведении ИВЛ. В динамике развилась анемия смешанного генеза тяжелой степени и тромбоцитопения. Уровень сознания — оглушение. На осмотр реагировал двигательной активностью, плачем, быстро истощался. Сохранялась диффузная мышечная гипотония, гипорефлексия. Менингеальной и очаговой неврологической симптоматики не отмечалось. Большой родничок 0,5×0,5 см, нормотоничен. Кожные покровы были бледные, чистые, имелись периоральный и периорбитальный цианоз, цианоз кистей и стоп, сниженная эластичность кожи. Подкожно-жировой слой был развит умеренно. Тургор тканей в норме. Периферические лимфоузлы не пальпировались. Периферических отеков не отмечалось. Слизистая оболочка полости рта была бледнорозовая, чистая, гиперемия зева. Дыхание через нос было затруднено, серозное отделяемое. Грудная клетка цилиндрической формы, не деформирована. При дыхании отмечалось втяжение уступчивых мест, участие в акте дыхания дополнительной мускулатуры. Дыхание кряхтящее. ЧД 96 в мин. Одышка смешанного характера с преобладанием экспираторного компонента. Перкуторно над легкими коробочный звук. Аускультативно дыхание жесткое, ослабленное в нижних отделах. С обеих сторон выслушивались мелкопузырчатые влажные хрипы, проводящиеся во все отделы. Тоны сердца приглушены, ритм правильный, шумы не выслушивались. ЧСС 170 в мин. Живот умеренно вздут, доступен глубокой пальпации, безболезненный. Печень +7 см, селезенка +2 см из-под края реберной дуги. Стул и мочеиспускание не нарушены.
Лабораторный данные: клинический анализ крови от 02.09.2015 — гемоглобин 123 г/л, эритроциты 4,61×1012/л, гематокрит 38%, тромбоциты 298×109/л, лейкоциты 13,4×109/л, палочкоядерные нейтрофилы 1%, сегментоядерные нейтрофилы 86%, эозинофилы 0, лимфоциты 8%, моноциты 6%, СОЭ 2 мм/ч. Биохимический анализ крови от 02.09.2015: белок 57,2 г/л, альбумин 27,5 г/л, АЛАТ 89 Ед/л, АСАТ 132 Ед/л, глюкоза 8,9 ммоль/л, билирубин 4,0 ммоль/л, мочевина 5,3 ммоль/л, креатинин 43,7 мкмоль/л, калий 4,0 ммоль/л, натрий 133 ммоль/л, хлор 96 ммоль/л, кальций 2,17 ммоль/л, железо 15,8 мкмоль/л, СРБ 54 мг/дл. Анализ мочи в норме.
Исследование крови на антитела HIVI методом ИФА: иммуноблот от 03.09.2015 положительный. Анализ крови на РНК HIVI методом ПЦР от 03.09.2015, результат: положительный, вирусная нагрузка 254 144 копий в 1 мл. Анализ крови от 04.09.2015 HBsAg и антиHCV не обнаружены.
Микроскопия мокроты на пневмоцисты 07.09.2015: в мокроте обнаружено большое количество скоплений пневмоцист.
Результат бактериологического исследования микрофлоры из зева от 16.09.2015: выделен Enterococcus faecalis обильный рост. Результат бактериологического исследования микрофлоры мокроты от 23.09.2015: выделен Enterococcus faecalis. Результат бактериологического исследования микрофлоры мокроты от 06.10.2015: выделена Burkholderia cepacia. ПЦР промывных вод бронхов и мазка из зева на диагностику туберкулеза от 10.09.2015: отрицательный.
Результаты анализа крови методом ИФА на группу инфекций от 04.09.2015: выявлены IgG-антитела в диагностическом титре к Cytomegalovirus hominis, Herpes simplex virus I, II, антитела к хламидофиле пневмонии и микоплазме пневмонии не обнаружены.
Иммунограмма от 04.09.2015: лимфопения, нейтрофилия; количество популяции общих зрелых Т-лимфоцитов (CD3+CD19-) существенно снижено (62%) при резком снижении иммунорегуляторного индекса (CD4+/CD8+) за счет дефицита субпопуляции Т-хелперов (CD3+CD4+) 2,7% (дефицит 93%). Содержание популяции натуральных киллеров — NKклеток (CD3-CD56+) существенно снижено (0,05109 л). Повышен уровень сывороточных иммуноглобулинов IgM и IgA.
ЭКГ от 03.09.2015: синусовая тахикардия, отклонение ЭОС вправо.
ЭХО-КГ от 02.09.2015: ЛЖ КДР 21 мм, КСР 14 мм, ФВ 72%. ООО 3 мм, расчетное давление в легочной артерии до 20/8 мм рт.ст.
УЗИ органов брюшной полости от 03.09.2015. Гепатомегалия, диффузное уплотнение структуры печени. Уплотнение стенок сосудов печени. УЗИ почек от 03.09.2015. Патологии не выявлено.
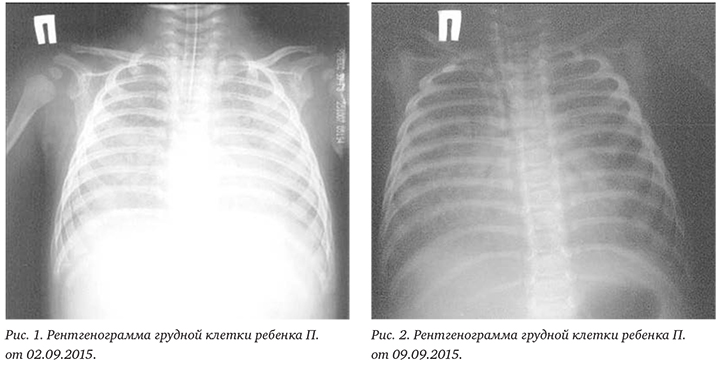
На рентгенограмме органов грудной клетки от 02.09.2015 признаки двухсторонней полисегментарной пневмонии (рис. 1).
На основании анамнеза, клинической картины и проведенного обследования ребенку был поставлен клинический диагноз: «ВИЧинфекция стадии 4В. Стадия вторичных заболеваний, тяжелый иммунодефицит. (СПИД). Внебольничная двусторонняя пневмония смешанной этиологии (пневмоцистной, бактериальной). Осложнения: Синдром полиорганной недостаточности: ДВС-синдром, ДН III степени. НК II АБ ст., острая печеночная недостаточность. Инфекционный токсикоз. Постнатальная гипотрофия 1 ст. Сопутствующие заболевания: Последствия перинатального поражения ЦНС гипоксически-ишемического генеза, в анамнезе родовая травма — перелом правой теменной кости. Кефалогематома правой теменной кости».
Получал интенсивное лечение с включением комбинации 3 антиретровирусных препаратов, антибактериальных препаратов (сочетание антибиотиков широкого спектра и бисептола из расчета 20 мг/кг по триметоприму длительным курсом), противогрибковой, инфузионной терапии, глюкокортикостероидов, симптоматической терапии.
На фоне проводимой терапии отмечалась незначительная стабилизация состояния, уменьшение кислородозависимости (концентрации кислорода до 60—65%) и, как следствие, смягчение параметров ИВЛ. Однако с 07.09.2015 состояние ребенка с отрицательной динамикой: отмечалась стойкая гектическая лихорадка на фоне выраженного интоксикационного синдрома. Лихорадка трудно поддавалась коррекции, усилилась кислородозависимость, потребовавшая ужесточения параметров ИВЛ, и потребность в более высоких концентрациях кислорода (80—85%). В динамике развилась анемия тяжелой степени и тромбоцитопения. 08.09.2015 зарегистрирован эпизод легочного кровотечении, снижение сатурации кислорода до 48%, при санации эндотрахеальной трубки алая кровь. С целью коррекции анемии и тромбоцитопении проведена трансфузия эритроцитарной взвеси O(I) Rh положительная и концентрата тромбоцитов в возрастных дозировках. Проведена гемостатическая терапия: перелита свежезамороженная плазма O(I) Rh положит. Продолжена ИВЛ на жестких параметрах: ЧД — 50 в мин; T вд. — 0,55 с, PееP — 5 мбар, PIP — 22 мбар, FiO2 — 80—100%. На этом фоне сатурация кислорода сохранялась на уровне 30—45%. Легочное кровотечение было расценено как следствие деструкции легочной ткани на фоне тяжелого течения пневмонии, ДВС-синдрома.
При контрольном рентгенологическом исследовании органов грудной клетки от 09.09.2015 пневматизация легочных полей ухудшилась. Легочный рисунок на фоне перибронхиальной инфильтрации слабо дифференцируется. Синусы свободны. Контуры диафрагмы и тень сердца четко не визуализируются. Интубационная трубка на уровне бифуркации.
С 11.09.2015 у ребенка трижды отмечались эпизоды желудочно-кишечного кровотечения (обильная рвота по типу «кофейной гущи», стул по типу мелены) с развитием тяжелой анемии, купированные проведением консервативной гемостатической и заместительной терапии (промывание желудка аминокапроновой кислотой, в/в введение аминокапроновой кислоты, трансфузия одногруппной свежезамороженной плазмы, переливание эритроцитарной взвеси O(I) Rh положительной). В динамике показатели ИВЛ были несколько смягчены: ЧД 50×40 в мин; FiO2 86×50%. С 07.10.2015 переведен на nCPAP, с 10.10.2015 переведен на полное спонтанное дыхание с дотацией увлажненным кислородом в объеме 2 л/мин через назальные канюли.
На фоне проводимой терапии состояние ребенка с положительной динамикой за счет купирования синдрома полиорганной недостаточности, ДВС-синдрома, тяжелой анемии, инфекционного токсикоза, метаболических нарушений, отечного синдрома, уменьшения проявлений недостаточности кровообращения и дыхательной недостаточности до 1—2 степени. При повторном обследовании на фоне лечения пневмоцисты в мокроте не выявлены, снизилась вирусная нагрузка РНК HIVI до 1316 копий/мл. При рентгенологическом обследовании отмечено улучшение пневматизации легочных полей, уменьшение воспалительной инфильтрации.
После стабилизации состояния ребенок 14.10.2015 был переведен на долечивание в специализированное отделение ИКБ № 2, где, несмотря на проводимое лечение, ребенок умер через 2 нед.
Таким образом, приведенное клиническое наблюдение демонстрирует, что у детей грудного возраста с ВИЧ-инфекцией при отсутствии адекватного контроля и профилактики пневмоцистная пневмония протекает остро и очень тяжело, с выраженной дыхательной недостаточностью, часто сочетается с другими инфекциями, осложняется развитием полиорганной недостаточности, ДВС-синдрома, легочного кровотечения и заканчивается летальным исходом.
- Пневмонии. Особенности диагностики, клиники, лечения внебольничной пневмонии. Ошибки лече- ния. М.: РНИМУ им. Н.И Пирогова, 2011: 127—154.
- Ватутин Н.Т., Колесников В.С., Тараторина А.А. и др. Особенности течения пневмонии у ВИЧ- инфицированных пациентов. Архивъ внутренней медицины. 2016;1(27):71—76.
- Ермак Т.Н., Литвинова Н.Г., Самитова Э.Р. и др. Пневмоцистная пневмония в сочетании с туберкуле- зом как первые клинические проявления на поздних стадиях ВИЧ-инфекции (заметка из практики). Тер. арх. 2005;11:21—23.3.
- Зюзя Ю.Р., Пархоменко Ю.Г., Зимина В.Н., Тишкевич О.А. Морфологические особенности пневмоцист- ной пневмонии при ВИЧ инфекции. Пульмонология.2012;5:56—61.
- Carmona E.M., Limper A.H. Update on the Diagnosis and Treatment of Pneumocystis Pneumonia. Ther. Adv. Resp. Dis. 2011;5(1):41—59.
- Grubman S., Simonds R.J. Preventing Pneumocystis carinii pneumonia in human immunodeficiency virus- infected children: new guidelines for prophylaxis. Pediatr. Infect. Dis.J. 1996;15:165—168.
- Huang L., Morris A., Limper A.H. et al. An Official ATS Workshop Summary: Recent Advances and Future Directions in Pneumocystis Pneumonia (PCP). Proc. Am. Thorac. Soc. 2006;3(8):655—664.
- Panel on Opportunistic Infections in HIV-Infected Adults and Adolescents. Guidelines for the prevention and treatment of opportunistic infections in HIV-infected adults and adolescents: recommendations from the Centers for Disease Control and Prevention, the National Institutes of Health, and the HIV Medicine Association of the Infectious Diseases Society of America. Available at https://aidsinfo.nih. gov/contentfiles/ lvguidelines/adult_oi.pdf.
Источник
