Лечение ожога вен после химиотерапии
Восстановление после химиотерапии должно быть не полностью самопроизвольным, растянутым на месяцы процессом с неизвестными результатами. В любом случае через некоторое время неприятности лекарственного противоопухолевого лечения существенно уменьшатся, но восстановление пойдет быстрее и успешнее только под контролем врача, а лучше команды специалистов, отлично разбирающихся во всех аспектах реабилитации онкологических пациентов.
Причины появления синяков
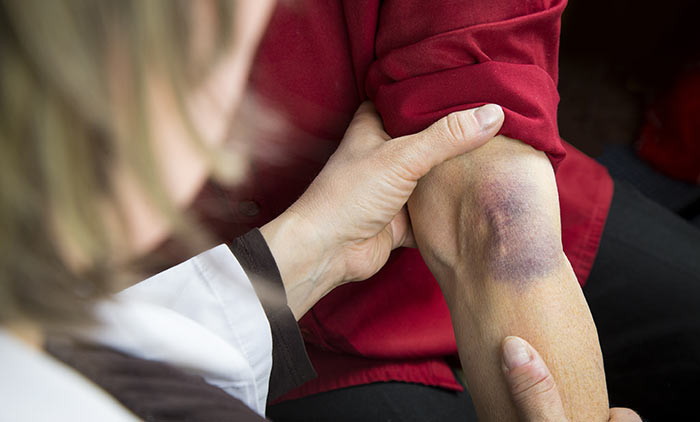
Синяк или гематома у онкологических больных встречаются часто, потому что химиотерапия связана с внедрением в организм посредством разрушения кожных покровов — внутривенными введениями лекарств, что не всегда удается без кровоизлияния в кожу и клетчатку вокруг сосуда. Противоопухолевые лекарства изменяют состав крови, в частности численность тромбоцитов, увеличивая кровоточивость, а также впятеро повышают вероятность образования тромбов, тогда как хронически существующая варикозная болезнь увеличивает тромбообразование всего лишь вдвое.
Злокачественная опухоль меняет реологические свойства крови, приводя к образованию тромбов. У каждого пятого пациента ещё до операции выявляют скрытый тромбоз. При раке кишечника и поджелудочной железы обильное образование тромбов может быть первым признаком злокачественного заболевания. Химиотерапия, как и метастатическая стадия любой опухоли, увеличивает вероятность тромбоза в среднем в пять раз. В организме онкологического больного одновременно сосуществуют два процесса — избыточная кровоточивость и повышенная свертываемость.
Факторы риска тромбозов у онкобольных как у всех «обычных» людей: большой вес и возраст «после 40», хронические болезни сосудов и сердца, сахарный диабет, гипертония и конечно варикозная трансформация вен нижних конечностей.
К этим стандартным причинам у онкологического пациента примешиваются специфические, то есть инициируемые злокачественной опухолью и усугубляемые необходимым лечением:
- сдавливание опухолевым конгломератом кровеносных и лимфатических сосудов;
- лимфостаз после удаления подмышечных лимфоузлов, в результате облучения или удаления клетчатки малого таза с лимфоузлами, а также блок метастатическим паховыми узами оттока лимфы из ноги;
- длительный приём гормональных препаратов;
- стимуляция красного ростка кроветворения эритропоэтинами;
- постоянно установленный для частых вливаний лекарств венозный катетер;
- вынужденное из-за слабости ограничение подвижности;
- операции и облучение, а также побочные эффекты химиотерапии на сосуды и форменные элементы крови.
Для инициации тромба внутри сосуда больному раком достаточно всего трёх поводов и не обязательно сразу всех:
- повреждение внутренней оболочки сосуда, что для обычно для внутривенной химиотерапии;
- застой крови, что называют «нарушением кровообращения», в том числе в результате опухолевого конгломерата;
- избыточная свертываемость вместе с нарушением формирования сгустков.
Симптомы воспаления вен после химиотерапии
Большинство химиопрепаратов применяется только в растворе, не в таблетках, что объясняется нестойкостью лекарственных молекул к желудочному соку и сильнейшим раздражающим действием цитостатика на слизистые оболочки желудочно-кишечного тракта. При непосредственном контакте цитостатика с венозной стенкой происходит его проникновение в клетки эндотелия с изменением структуры ДНК. Произошедшая химическая реакция направляет эндотелиальную клетку к воспалительным изменениям либо к смерти — апоптозу. Повреждение усугубляется травмой стенки вены инъекционной иглой или катетером.
Воспаление венозной стенки — флебит, к которому быстро подключаются факторы риска образования тромбов, и в поврежденной химиотерапией вене развивается тромбофлебит.
Флебит проявляется болью, причём в процессе введения цитостатика боль может быть очень интенсивной, и не только в месте инъекции, но по всей руке, когда больной как будто ощущает движение лекарства по сосудистой сети, так и говорят, что «вена горит». Боль может быть краткой, а может остаться на несколько дней и даже неделю, зависит это не только от выраженности ожога эндотелия, но и личностных особенностей больного по восприятию болевых ощущений.
Боль при прохождении лекарства приводит к спастическому сокращению вены, в ответ на которое расширяются впадающие в неё мелкие венки, на внутренней поверхности руки появляется сеточка из расширенных синих сосудиков на фоне побледневшей из-за спазма артериол кожи.
Воспаленную вену можно прощупать, она как тяж плотная из-за местной отечности тканей. Когда в просвете сосуда возникнет тромб, его тоже можно будет нащупать и увидеть при УЗ- дуплексном сканировании.
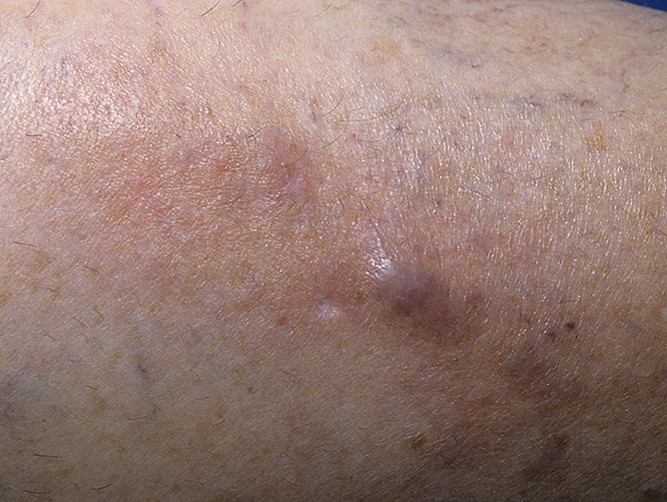
Со временем воспаление пройдет, уплотнение сосуда может остаться, кожа над ним может потемнеть. Внутренний просвет сосуда после нескольких химиотерапевтических ожогов уменьшится вплоть до закрытия — облитерации. За время течения флебита откроются и расширятся подходящие к больной вене мелкие сосудики — коллатерали, но останется вероятность небольшой отечности руки ниже места венозного повреждения.
Основные методы лечения вен
После внедрения цитостатика внутрь клеток остается только ждать завершения побочного процесса и помогать восстановлению.

Патофизиология лекарственного токсического флебита мало изучена, клинических исследований по проблеме не проводилось, все рекомендации базируются только на личном опыте медицинского персонала. В каждом случае и после каждого введения необходимо консультироваться с лечащим врачом, знающим особенности локального взаимодействия цитостатика и спектр местных побочных реакций.
Для купирования болевого синдрома и уменьшения воспаления лучше всего подходят НПВС — нестероидные противовоспалительные средства, но не доказано преимуществ какого-либо одного препарата, лучше опираться на «житейские» предпочтения пациента, потому что и чувствительность к боли разная, и обезболивающий эффект тоже индивидуален.
При высоком риске легочной тромбоэмболии пациенту назначается специальная — «разжижающая кровь» терапия, как правило, длительная — никак не менее недели и при регулярном контроле свертываемости.
Можно использовать мази с гепарином для втирания в зону поврежденного сосуда. Любимый пациентами гель Гепатромбин™ состоит из гепарина и преднизолона, последний имеет противовоспалительное действие, препарат официально не сертифицирован для использования при периферическом флебите и тромбофлебите.
Хорошая репутация у мази Троксевазин™ (троксерутин), одновременно уменьшающей воспаление и отечность тканей, изменяющей реологические свойства крови в сторону разжижения, но меньше, чем это присуще гепарину. Тем не менее, исследования показали, что препарат способен растворять микротромбы.
Гель Индовазин™ представляет смесь троксерутина и НПВС индометацина, поэтому уменьшает выраженность боли и делает всё, что присуще Троксевазину™. Нецелесообразно сочетать обе мази, поскольку спектр действий комбинированного препарата больше, но с Индовазином™ вполне можно чередовать нанесение Гепатромбина™. Всасывание мазей микроскопическое, они не подменяют собой принимаемые внутрь НПВС и антикоагулянты, но помогают перенести неприятные последствия лечения.
Как восстанавливаются вены после капельниц: полезные процедуры
Местное раздражение слизистой, выстилающей внутреннюю стенку вены, пытаются уменьшить большим разведением и медленным введением в капельницах, буквально часами. Не все цитостатики выдерживают большое разведение и долгое введение, некоторые теряют свои свойства, поэтому их вводят болюсно — шприцем. В этом случае сразу же после химиопрепарата вену «моют» физиологическим раствором, стараясь уменьшить её повреждение.
Обязательно до введения и в процессе капельницы неоднократно проверяется проходимость сосуда и возможность экстравазации — распространение цитостатика в клетчатке при микроскопических разрывах сосудистой стенки.
Рекомендуется не делать химиотерапию в одну и ту же вену, лучше чередовать руки, давая сосуду больший срок на восстановление своей слизистой оболочки. Профилактическое использование мазей с гепарином или троксерутином до химиотерапии лишено патоморфологических оснований, то есть бесполезно.
При планировании многомесячной химиотерапии целесообразно подумать об установке венозного порта, срок его службы, как минимум, пятилетка. Устройство полностью исключает такой побочный эффект как лекарственный флебит, но от тромбозов спасает только приём антикоагулянтов.
Профилактика осложнений
Многие цитостатики повреждают вены, особенно усердны в инициации химических флебитов агрессивные цисплатин, антрациклины и винкаалкалоиды, а также сравнительно «мягкие» гемцитабин с фторурацилом. По действию на ткани антрациклины с винкаалкалоидами отнесены к кожно-нарывным, цисплатин всего лишь к раздражающим, а гемцитабин точно не кожно-нарывной. Тем не менее любой химиопрепарат, а тем более комбинация цитостатиков, способны повредить вену, поэтому во время внутривенного введения персонал должен строго исполнять инструкцию по длительности и способу инъекции.
Помогают восстановлению физиотерапевтические процедуры и акупунктура, фототерапия и инфракрасное облучение, стимуляция магнитным полем.
В нашей Клинике каждому больному проводится определённая и ориентированная на особенности организма и сопротивляемость тканей программа сопровождения химиотерапии и восстановления после лечения.
Список литературы:
- Российские клинические рекомендации по профилактике и лечению венозных тромбоэмболических осложнений у онкологических больных// М.: Планида; 2012
- Сомонова О.В., Антух Э.А., Елизарова А.Л., с соавтр. /Практические рекомендации по профилактике и лечению тромбоэмболических осложнений у онкологических больных // Злокачественные опухоли: Практические рекомендации RUSSCO #3s2; 2017 (том 7).
- Antithrombotic Therapy and Prevention of Thrombosis, 9th ed: American College of Chest Physicians Evidence-Based Clinical Practice Guidelines// Chest Am Coll Chest Phys.; 2012.
- Jones S., Holmes F., O´Shaughnessey J., et al. /Docetaxel with cyclophosphamide is associated with an overall survival benefit compared with doxorubicin and cyclophosphamide: 7-year follow-up of US Oncology Re trial 9735// JCO 2009; 27.
- International Society of Lymphology. The diagnosis and treatment of peripheral lymphedema: 2013 Consensus Document of the International Society of Lymphology// Lymphology; 2013 Mar; 46(1).
- Khorana A.A., Kuderer N.M., Culakova E., et al./ Development and validation of a predictive model for chemotherapy-associated thrombosis// Blood 2008; 15.
Источник
Введение химиотерапевтических препаратов, применяемых при лечении онкологических заболеваний, в большинстве случаев проводится через вены. Именно они страдают первыми, подвергаясь воздействию токсичных препаратов. Повреждающее действие цитостатиков усугубляется тем, что инъекции в одну и ту же вену проводятся многократно, в некоторых случаях – ежедневно.
При внутривенном введении цитостатических препаратов нередко развиваются венозные воспалительные реакции. Проявляются они разнообразно – от выраженной боли по ходу сосудов уже во время инъекции, до острых флебитов, тромбофлебитов, флеботромбозов.
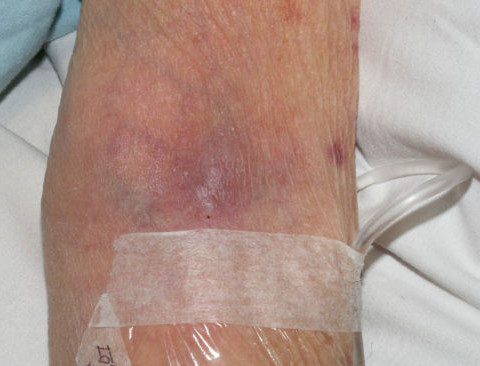
Какие нежелательные явления в области вен могут возникнуть при проведении химиотерапии?
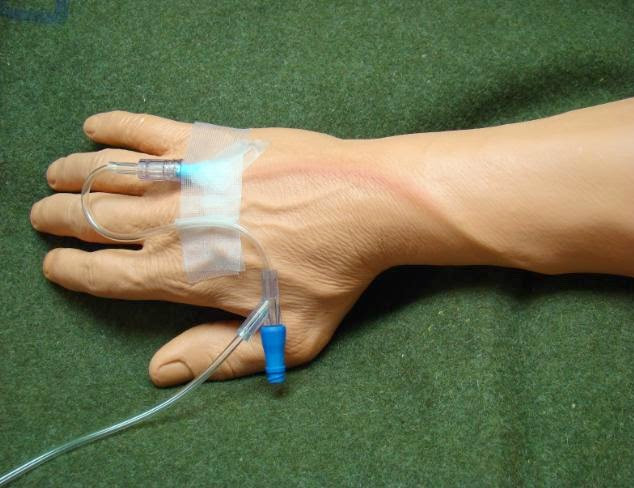
- Довольно часто уже во время введения препарата по ходу вен появляются зуд и покраснение. Что делать в этом случае?
Пациенту следует поднять руки и приложить тепло или холод к венам (в зависимости от вида вводимого лекарства). Чаще всего эти симптомы проходят примерно через 30 минут и не приводят к каким-либо осложнениям в дальнейшем.
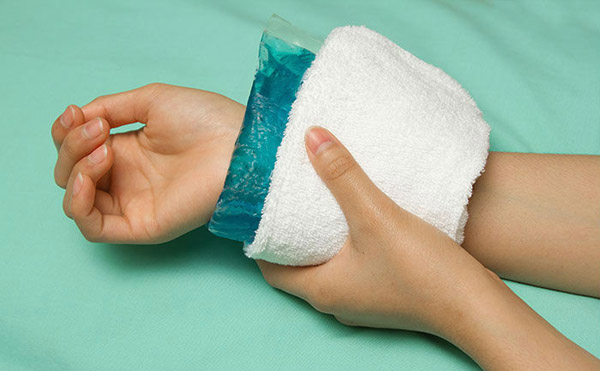
- В случае попадания цитостатика под кожу, при неправильном его введении, рука может потерять способность сгибаться или разгибаться полностью. То есть появляется контрактура – ограничение движения в зоне поражения тканей.
Необходимо сразу же, не вынимая шприц или катетер, попытаться извлечь препарат. Затем удалить иглу и ввести соответствующий препарату антидот.
- Раздражающие препараты, такие как цисплатин, дакарбазин, этопозид, фторурацил, паклитаксел, винорельбин, могут вызвать жгучую боль в месте инъекции, но не приводят к некрозам.
Препараты с кожно-нарывным действием — доксрубицин, эпирубицин, митомицин, винбластин, винкистин обычно вызывают сильную боль. В течение нескольких дней возможно появление отека, затем происходит уплотнение тканей. Через одну-четыре недели на коже могут появиться язвы и развиться некроз, то есть омертвение тканей. Самостоятельное заживление практически невозможно, пациенту необходимо обратиться за помощью к хирургу.
Любая химиотерапия должна проводиться только в специализированном отделении медицинского учреждения с соответствующей аккредитацией. Каждый препарат имеет свою сложную систему введения. Чтобы свести к минимуму побочные эффекты или предотвратить их появление, врачи и медсестры должны иметь необходимую подготовку и опыт работы с цитостатиками.
Венозные осложнения после проведения химиотерапевтического лечения
Довольно частыми осложнениями после курса химиотерапии являются болезни вен – флебиты. Это воспалительные процессы стенок кровеносных сосудов, которые иногда приводят к образованию тромбов и появлению тромбофлебита. В первую очередь это происходит у пациентов с плохим состоянием сосудов, у которых есть склонность к образованию тромбов.
Подготовка вен к химиотерапии и профилактика побочных эффектов
- Для проявления вен при их низкой доступности — серьезном препятствии для проведения терапии.
Пациентам рекомендуется пить больше воды и держать руки в тепле. Непосредственно перед процедурой химиотерапии помогут эспандер, теплые обертывания. Для создания компрессии врач может использовать манометр.
- Для снижения токсического воздействия препаратов на вены.
В этом случае инъекции раствора цитостатиков делаются в минимально допустимых концентрациях. Самый щадящий способ введения — капельная инфузия с большим количеством жидкости. При введении струйным методом, после инъекции требуется промывание вены изотоническим раствором .
Но не всегда есть возможно выбирать – каждый препарат имеет свою рекомендованную концентрацию, скорость введения и метод.
Инъекции химиопрепаратов должны проводиться попеременно в вены разных конечностей, если, опять-таки, существует такая возможность.
- Для снижения риска воспаления или отека.
Следующие 48 часов после химиотерапии рекомендуется как можно чаще держать «страдающую» конечность в приподнятом положении.

Лечение осложнений
В первую очередь, при поражении окружающих тканей, необходимо сообщить об этом своему химиотерапевту.
Различные методы самолечения могут лишь усилить химический ожог и привести к появлению язв.
При воспалениях и некрозах
Допускается применение теплого компресса, либо пакета со льдом в зависимости от типа препарата. Возможна аппликация гидрокортизоновой мази при наличии воспалительной реакции. Внимание! Перед лечением консультация с врачом обязательна.
В случае сохранения симптомов в течение двух и более дней, дальнейшим лечением таких осложнений занимается хирург. При затянувшихся более, чем на 10 дней некрозах, проводится иссечение омертвевших тканей с последующей пластикой дефекта.
При флебитах и тромбофлебитах
Лечение разросшихся флебитов и тромбофлебитов, вызванных введением цитостатиков, производится исключительно врачом и не отличается от лечения этих заболеваний, возникших вследствие других причин. Цель лечения состоит в том, чтобы уменьшить болезненность и убрать воспаление, а также предупредить развитие осложнений. Если тромбофлебит обусловлен катетером, то катетер необходимо удалить.
Использование венозного доступа для проведения химиотерапии
Для введения препарата в течение длительного времени, применяется установка специального устройства – венозного катетера, либо имплантируемого порта, что делает химиотерапию гораздо более щадящей процедурой для вен, снижает риск нежелательной «побочки».
Периферический венозный катетер сегодня является распространенным устройством в медицинских учреждениях Санкт-Петербурга. При адекватном уходе, установленный катетер можно применять до 7-10 дней. Эти устройства требуют тщательного ухода и промывки, а их многократная установка повышает риск занесения инфекции.
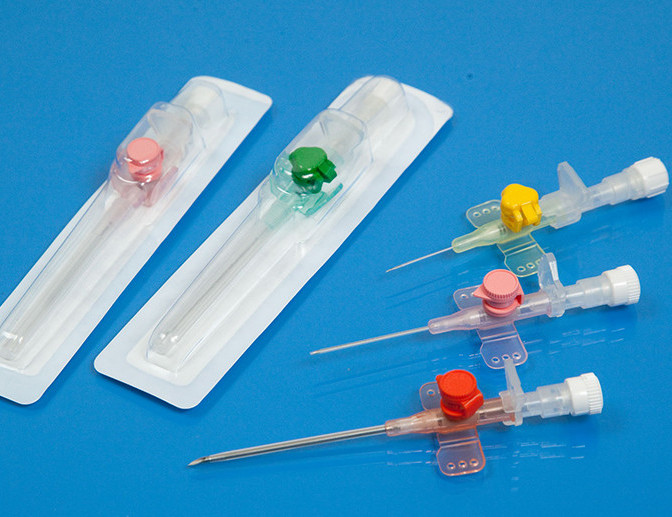
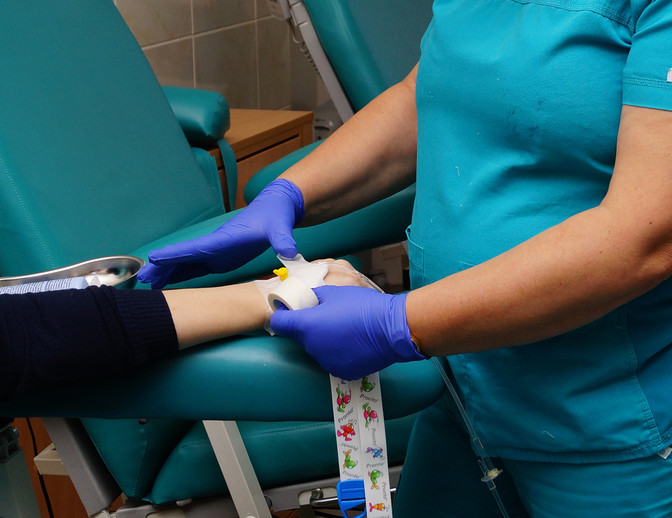
Центральный венозный катетер устанавливается на крупные вены и имеет очевидные преимущества: он может устанавливаться на длительное время, не ограничивает скорость и объем введения раствора, крупные вены легче усваивают препарат. В то же время растет риск инфицирования и усиливаются его последствия. Использование такого катетера предполагает повышенные требования к квалификации персонала и к уходу за устройством.

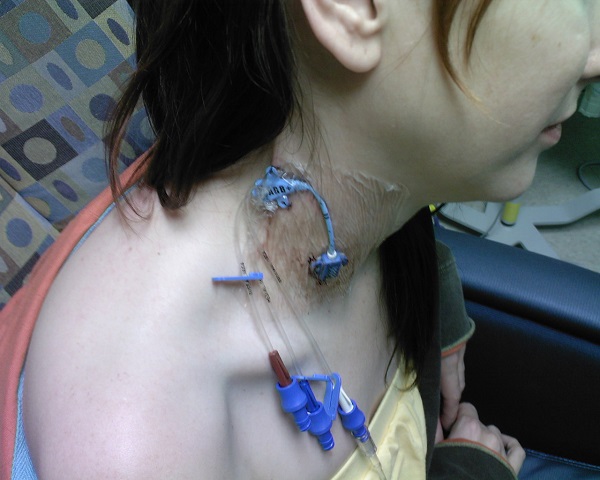
Имплантируемый венозный порт лишен многих недостатков катетеров. Это небольшое устройство, которое под местной анестезией устанавливается под кожу пациента (как правило, в правую подключичную область) и соединяется с яремной веной. При этом возраст и комплекция пациента не имеют значения. Размеры – всего 4 сантиметра в диаметре при толщине в 1 сантиметр. Внешняя часть устройства имеет силиконовую мембрану, через которую вводятся лекарственные препараты. Уход за портом предполагает использование для инъекций исключительно игл Губера и промывание физраствором после инфузии или забора крови. Такие иглы не повреждают силиконовую мембрану и позволяют провести до 2000 инъекций.
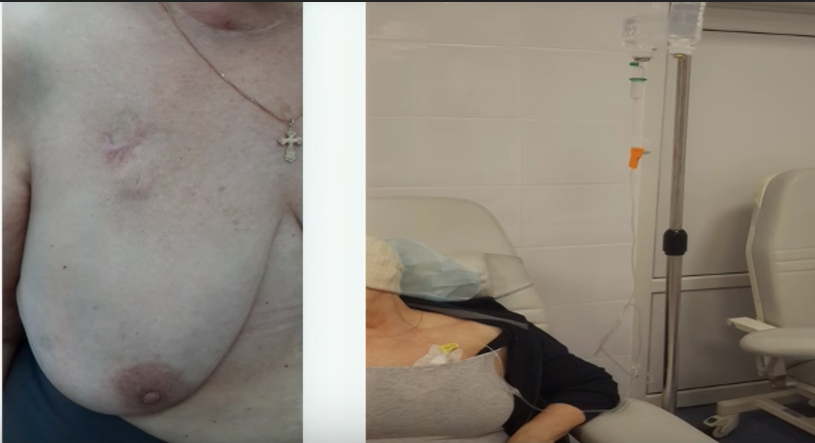
Порт не виден снаружи, не может случайным образом инфицироваться, его использование не накладывает ограничений на образ жизни пациента: можно плавать, заниматься спортом, проходить МРТ/КТ. Срок службы порта составляет 5-7 лет.
Порты широко используются в странах Западной Европы, когда планируется проведение множественных сеансов химиотерапии, особенно цитостатическими препаратами. В консультационно-диагностическом отделении НМИЦ онкологии им. Н.Н. Петрова уже сложилась практика установки венозных портов онкологическим пациентам, несмотря на то, что в отечественных онкологических учреждениях эти устройства используются, пока, довольно редко.
Источник
Что такое кожная токсичность?
Кожная токсичность – это кожные реакции, которые появляются более чем у 80% пациентов на фоне системной лекарственной противоопухолевой терапии. Эти реакции являются результатом токсического, угнетающего воздействия химиотерапии на растущие, быстроделящиеся клетки организма, в том числе клетки кожи, волос и ногтей. Так ранние реакции развиваются через 1-2 недели, отсроченные реакции через 3-5 недель и поздние реакции через 6 и более недель.
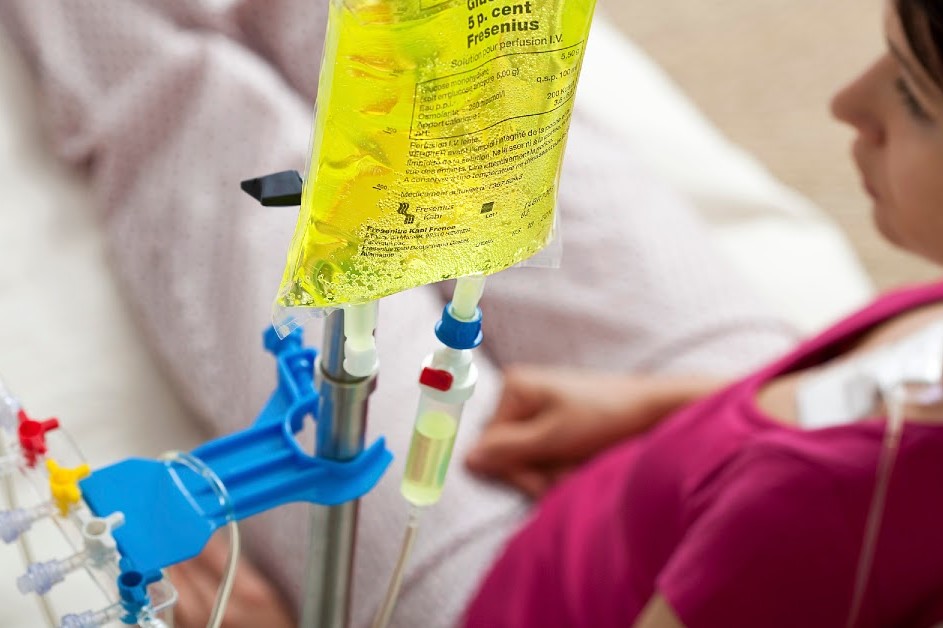
При химиотерапии кожа у пациента становится очень сухой, истончается, шелушится, трескается; может появляться кожный зуд. На лице, голове, туловище появляются акнеподобные (угревые) высыпания. На ладонях и подошвах кожа краснеет, грубеет, трескается, шелушится. На туловище и конечностях могут появляться высыпания в виде пятен и узелков. При попадании на кожу солнечных лучей могут возникать фотоаллергические реакции. Развивается выпадение волос, изменения ногтей и ногтевых валиков.
Типы кожной токсичности
К настоящему моменту описано более 30 различных вариантов кожной токсичности. Наиболее часто встречаются:
- акнеподобные (угревые) высыпания;
- ксероз (сухость, истончение, шелушение) кожи;
- кожный зуд;
- ладонно-подошвенная кожная реакция;
- ладонно-подошвенный синдром;
- пятнисто-папулезные высыпания (в виде пятен и узелков);
- фотореакции (патологические кожные реакции на солнце);
- изменения роста волос и ногтей;
- новообразования кожи и другие.
Химиотерапия, таргетная терапия и кожная токсичность
Для различных видов противоопухолевой терапии характерны свои особенности кожных реакций.
Так при химиотерапии (цитостатики) нарушаются процессы роста и механизмы деления всех клеток организма, а не только опухолевых. При этом происходит прямое цитотоксическое действие на клетки кожи и ее придатков, вследствие чего развиваются ладонно-подошвенный синдром, нарушение пигментации кожи, выпадение волос, изменение ногтей.
При таргетной терапии клетки кожи становятся «второй мишенью», помимо опухолевых клеток, так как несут на себе те же рецепторы, блокируемые препаратом. Например, препараты ингибиторы EGFR (эпидермального фактора роста) подавляют рост клеток кожи, волос и ногтей, вызывают выброс повреждающих тканевых ферментов и асептическое воспаление. В результате развиваются акнеподобные (угревые) высыпания, ксероз (сухость, истончение, шелушение) кожи, изменения волос и ногтей, поражение слизистых оболочек, ладонно-подошвенные кожные реакции, фотореакции (патологические кожные реакции на солнце).
Степень кожной токсичности
При оценке степени тяжести кожной токсичности учитывается площадь поражения, объективное ухудшение кожного процесса, выраженность субъективных ощущений пациента, нарушение его повседневной жизнедеятельности.
Так, например, по выраженности угревой (акнеподобной) сыпи выделяют 4 степени процесса:
I степень — площадь высыпаний менее 10%, возможен кожный зуд (болезненность);
II степень — площадь высыпаний 10-30%, кожный зуд (болезненность), негативное психологическое воздействие, ограничение активности;
III степень — площадь высыпаний более 30% кожный зуд (болезненность), негативное психологическое воздействие, ограничение самообслуживания, возможна локальная суперинфекция;
IV степень — площадь высыпаний любая связанная с распространенной суперинфекцией, требующей назначения внутривенной антибиотикотерапии, жизнеугрожающее состояние.
Таким образом, более тяжелые степени кожной токсичности требуют более активной терапии, снижения дозы химиопрепаратов, а при тяжелой III-IV степени приходится прерывать противоопухолевую терапию.
Первая помощь при кожной токсичности

Уже накануне противоопухолевой терапии врач-онколог назначает профилактическую терапию кожной токсичности, которая включает в себя:
- нанесение аптечных увлажняющих кремов-эмолентов утром;
- нанесение глюкокортикоидных кремов вечером (с активностью не выше 1% гидрокортизоновой мази);
- нанесение аптечных солнцезащитных кремов на открытые участки тела перед выходом на улицу в период с весны по осень (с фильтрами SPF>20, PPD>1/3 SPF)
- при таргетной терапии дополнительно назначаются антибиотики тетрациклинового ряда в противовоспалительной дозировке.
Если на фоне профилактической терапии проявления кожной токсичности все-таки прогрессируют, необходимо сообщить об этом лечащему врачу и получить консультацию врача-дерматолога (дерматовенеролога), который назначит дополнительное лечение кожной токсичности.
Кроме того, пациенты с наличием хронических кожных заболеваний должны получить консультацию врача-дерматолога еще перед началом курса химиотерапии.
Чем опасно отсутствие лечения кожной токсичности?
При отсутствии лечения кожной токсичности возможно развитие распространенной суперинфекции, тяжелого жизнеугрожающего состояния и прерывание курса системной лекарственной противоопухолевой терапии.
Как правильно ухаживать за кожей во время химиотерапии?

Полностью избежать кожной токсичности невозможно, но при помощи следующих профилактических мероприятий можно уменьшить ее интенсивность:
- использование мягких синдетных моющих средств, мягких полотенец;
- увлажнение кожи, кремы-эмоленты 2 раза в день;
- аптечные солнцезащитные кремы с максимальными фильтрами;
- исключение макияжа, травм, агрессивных процедур (обрезной маникюр, электробритвы и др.)
- рекомендован аппаратный медицинский педикюр в подологическом кабинете;
- ограничить физические нагрузки на стопы и пальцы кистей;
- ношение головных уборов, просторной мягкой хлопчатобумажной одежды;
- ношение просторной и удобной обуви с ортопедическими стельками;
- пользоваться хлопчатобумажными защитными перчатками;
- избегать воздействия бытовой химии, раздражителей и спиртовых растворов;
- ограничить водные процедуры (горячий душ, ванны, баня);
- в рационе питания должны быть продукты богатые кальцием, железом, цинком, витаминами А, Е и омега 3-6-9 жирными кислотами;
- при наличии заболеваний кожи, ногтей и волос, либо если такие проблемы были ранее, необходимо получить консультацию врача-дерматолога (дерматовенеролога)
Что делать, если возникает зуд?
Если пациент получает профилактическую терапию кожной токсичности: увлажняющие кремы-эмоленты утром, 1% гидрокортизоновый крем вечером, солнцезащитный крем и все-таки возникает зуд, — следует обратиться к лечащему врачу, либо на консультацию врача-дерматолога (дерматовенеролога).
Для облегчения зуда можно дополнительно нанести на зудящие области кремы-эмоленты. Внутрь можно принять 1 таблетку антигистаминного препарата 2-го поколения.
Что делать, если возникает сыпь?
Если пациент применяет профилактическую терапию кожной токсичности и при этом развивается сыпь, следует обратиться к лечащему врачу, который оценит степень тяжести, назначит дополнительное лечение, либо консультацию врача-дерматолога (дерматовенеролога).
Что делать, если поднялась температура?
Следует сообщить об этом лечащему врачу. При повышении температуры тела выше 38 гр. необходимо принять внутрь нестероидный противовоспалительный препарат.
Что делать, если есть сухость и шелушения?
Сухость и шелушение хорошо корректируются при помощи кремов-эмолентов, которые можно наносить 2 и более раз в сутки.
Что делать, если кожа меняет цвет?
Гиперпигментация кожи обычно развивается через 2–3 недели после окончания химиотерапии или на 10–12 неделе после начала курса лечения. Появляются окрашенные пятна на кончиках пальцев, локтевых суставах или ладонях, лице, вдоль используемых для инъекции вен.
Гиперпигментация дополнительного лечения не требует. После окончания курса противоопухолевой терапии она постепенно исчезнет. Специфической профилактики нет.
Как вести себя на солнце во время проведения курса химиотерапии?
Необходимо исключить пребывание на солнце. Рекомендовано ношение одежды с длинным рукавом, головной убор с широкими полями, солнцезащитные очки. Для верхней одежды предпочтение следует отдавать льняным тканям как более эффективным в отношении солнцезащиты, чем хлопчатобумажные. При этом окрашенные ткани обладают большим защитным эффектом по сравнению с белыми. Кроме того, нейлон, шерсть и полиэстер лучше защищают от ультрафиолетового облучения, чем хлопок.
Даже в холодные периоды года и при отсутствии солнца за 20 мин до выхода на улицу рекомендуется наносить на открытые участки кожи (лицо, кисти и др.) аптечные солнцезащитные кремы с максимальной комплексной защитой: SPF 50+/PPD 46.
Что при кожной токсичности категорически нельзя делать?
Нельзя заниматься самолечением кожной токсичности, в том числе народными средствами и самостоятельно снижать дозу, либо отменять противоопухолевые препараты.
Список литературы:
- Каспаров Б. С., Рогачев М. В., Беляев А. М. и соавт. Амбулаторная онкология. Практические аспекты (Часть 2). Учебное пособие. — Санкт-Петербург: «Грейт Принт», 2020. – 161 с.
- Жуков Н. В. Практическое пособие по сопроводительной терапии в онкологии.— М.: Литтерра, 2008.— 44 с.
- Практические рекомендации Российского общества клинической онкологии.— 2018 г. [Electronic resource]. URL: https://rosoncoweb.ru/standarts/RUSSCO/2019/ (accessed: 20.07.2019)
- Проценко С. А., Антимоник Н. Ю., Берштейн Л. М., Новик А. В. и др. Практические рекомендации по коррекции иммуноопосредованных нежелательных явлений // Злокачественные опухоли: Практические рекомендации RUSSCO.— 2017.— Т. 7, №3.— С. 592-620 5. Проценко С. А., Антимоник Н. Ю., Берштейн Л. М., Новик А. В., Носов Д. А., Петенко Н. Н. и др. Практические рекомендации по управлению иммуноопосредованными нежелательными явлениями // Злокачественные опухоли: Практические рекомендации RUSSCO.— 2018.— Т. 8, № 3.— С. 636–665.
- Российское общество клинической онкологии. Злокачественные опухоли — 2019.— Vol. 9 — P.655–667, P.678–684.
- Alimonti A. et al. Nail disorders in a woman treated with ixabepilone for ic breast cancer // Anticancer Res.— 2005.— Vol. 25, № 5.— P. 3531–3532.
- Alley E., Green R., Schuchter L. Cutaneous toxicities of cancer therapy // Curr. Opin. Oncol.— 2002.— Vol. 14, № 2.— P. 212–216.
- Autier J. et al. Prospective study of the cutaneous adverse effects of sorafenib, a novel multikinase inhibitor // Arch. Dermatol.— 2008.— Vol. 144, № 7.— P. 886–892.
- Balagula Y. et al. Clinical presentation and management of dermatological toxicities of epidermal growth factor receptor inhibitors // Int. J. Dermatol.— 2011.— Vol. 50, №2.— P. 129–146 49. Balagula Y., Rosen S. T., Lacouture M. E. The emergence of supportive oncodermatology: The study of dermatologic adverse events to cancer therapies // J. Am. Acad. Dermatol.— 2011.— Vol. 65, № 3.— P. 624–635.
- Batchelor D. Hair and cancer chemotherapy: consequences and nursing care a literature study // Eur. J. Cancer Care (Engl).— 2001.— Vol. 10, № 3.— P. 147–163.
- Bolognia J. L., Cooper D. L., Glusac E. J. Toxic erythema of chemotherapy: A useful clinical term // J. Am. Acad. Dermatol.— 2008.— Vol. 59, № 3.— P. 524–529.
- Bonamichi-Santos R., Castells M. Diagnoses and Management of Drug Hypersensitivity and Anaphylaxis in Cancer and Chronic Inflammatory Diseases: Reactions to Taxanes and Monoclonal Antibodies // Clin. Rev. Allergy Immunol.— 2016.
- Busam K. J. et al. Cutaneous side-effects in cancer patients treated with the antiepidermal growth factor receptor antibody C225 // Br. J. Dermatol.— 2001.— Vol. 144, № 6.— P. 1169–1176 .
- Chen P., Chen F., Zhou B. Systematic review and -analysis of prevalence of dermatological toxicities associated with vemurafenib treatment in patients with melanoma // Clin. Exp. Dermatol.— 2019.— Vol. 44, № 3.— P. 243–251.
- Choi J. N. Chemotherapy-induced iatrogenic injury of skin: new drugs and new concepts // Clin. Dermatol.— 2011.— Vol. 29, № 6.— P. 587–601.
- Chon S. Y. et al. Chemotherapy-induced alopecia // J. Am. Acad. Dermatol.— 2012.— Vol. 67, № 1.— P. 37–47.
- Degen A. et al. The hand-foot-syndrome associated with medical tumor therapy — classification and management // J. Dtsch. Dermatol. Ges.— 2010.— Vol. 8, № 9.— P. 652–661.
- Dueland S. et al. Epidermal growth factor receptor inhibition induces trichomegaly // Acta Oncol.— 2003.— Vol. 42, № 4.— P. 345–346.
- Fischer A. et al. The risk of hand-foot skin reaction to axitinib, a novel VEGF inhibitor: a systematic review of literature and -analysis // Invest New Drugs.— 2013.— Vol. 31, № 3.— P. 787–797.
- Hu J. C. et al. Cutaneous side effects of epidermal growth factor receptor inhibitors: clinical presentation, pathogenesis, and management // J. Am. Acad. Dermatol.— 2007.— Vol. 56, № 2.— P. 317–326.
- Gressett S. M., Stanford B. L., Hardwicke F. Management of hand-foot syndrome induced by capecitabine // J. Oncol. Pharm. Pract.— 2006.— Vol. 12, № 3.— P. 131–141 71. Gutzmer R. et al. Management of cutaneous side effects of EGFR inhibitors: ations from a German expert panel for the primary treating physician // J. Dtsch. Dermatol. Ges.— 2011.— Vol. 9, № 3.— P. 195–203.
- Kouwenhoven T. A., van de Kerkhof P. C. M., Kamsteeg M. Use of oral antidepressants in patients with chronic pruritus: A systematic review // J. Am. Acad. Dermatol.— 2017.— Vol. 77, № 6.— P. 1068–1073.
- Lacouture M. E. et al. Clinical practice guidelines for the prevention and treatment of EGFR inhibitor-associated dermatologic toxicities // Support Care Cancer.— 2011.— Vol. 19, № 8.— P. 1079–1095.
- Lacouture M. E. et al. Evolving strategies for the management of hand-foot skin reaction associated with the multitargeted kinase inhibitors sorafenib and sunitinib // Oncologist.— 2008.— Vol. 13, № 9.— P. 1001–1011.
- Lee M.-W. et al. Cutaneous side effects in non-small cell lung cancer patients treated with Iressa (ZD1839), an inhibitor of epi-dermal growth factor // Acta Derm. Venereol.— 2004.— Vol. 84, № 1.— P. 23–26.
- Mangili G. et al. Prevention strategies in palmar-plantar erythrodysesthesia onset: the role of regional cooling // Gynecol. On-col.— 2008.— Vol. 108, № 2.— P. 332–335.
- Matsuda K. M. et al. Gabapentin and pregabalin for the treatment of chronic pruritus // J. Am. Acad. Dermatol.— 2016.— Vol. 75, № 3.— P. 619–625.
- Masters J. C., Nickens D. J., Xuan D., Shazer R. L., & Amantea M. Clinical toxicity of antibody drug conjugates: a -analysis of payloads // Investigational New Drugs.— 2017.— № 36.— Р. 121–135 100. McGarvey E. L. et al. Psychological sequelae and alopecia among women with cancer // Cancer Pract.— 2001.— Vol. 9, № 6.— P. 283–289.
- McLellan B. et al. Regorafenib-associated hand–foot skin reaction: practical advice on diagnosis, prevention, and management // Ann. Oncol.— 2015.— Vol. 26, № 10.— P. 2017–2026.
Источник
