Последствия ивл при пневмонии у новорожденных
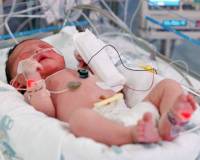
Пневмония у новорожденных — это острое инфекционно-воспалительное поражение респираторных отделов легких. Основные причины: возбудители TORCH-комплекса, стрептококки и стафилококки, хламидии, другие патогены, колонизирующие родовые пути матери. Заболевание проявляется синдромом дыхательных расстройств, инфекционным токсикозом, неврологическими нарушениями. Для диагностики неонатальных пневмоний проводят рентгенографию ОГК, бакпосев мокроты, серологические и общеклинические исследования крови. Лечение включает этиотропную антибиотикотерапию, кислородную поддержку, патогенетические медикаменты (иммуномодуляторы, инфузионные растворы).
Общие сведения
Пневмония — одна из основных проблем практической неонатологии. Заболеваемость составляет около 1% среди доношенных новорожденных и до 10% среди недоношенных. У младенцев, которые сразу после рождения находились на длительной ИВЛ, распространенность нозокомиальной пневмонии составляет до 40-45%. Воспаление легких рассматривается в качестве основной причины или сопутствующего фактора до 25% летальных исходов в период неонатальности. По данным Росстата, младенческая смертность от пневмонии достигает 7,5%.

Пневмония у новорожденных
Причины
У новорожденного собственный иммунитет крайне низкий, а все системы органов находятся в состоянии транзиторных приспособительных реакций и еще не адаптировались к смене условий после рождения. Поэтому младенцы очень чувствительны к любым видам инфекций, от которых преимущественно страдают кожа и респираторный тракт. Этиологическая структура неонатальных пневмоний отличается от таковой у старших детей и взрослых. Конкретные причины зависят от пути заражения:
- Трансплацентарный. В утробе матери ребенок чаще сталкивается с инфекциями TORCH-комплекса, которые имеют тропность к эпителию дыхательных путей, — с краснухой, токсоплазмозом, простым герпесом и цитомегаловирусом. В редких случаях происходит заражение сифилисом и туберкулезом.
- Интранатальный. Во время родов основной путь инфицирования — контактный, который реализуется при прохождении через материнские родовые пути. Если они не санированы, новорожденный может заразиться хламидиями, кишечной палочкой микоплазмой и уреаплазмой. Чаще других встречается хламидийная пневмония (33% случаев).
- Постнатальный. После рождения заражение младенца может произойти в стационаре, особенно, если ему проводят инвазивные манипуляции или кислородную поддержку. Здесь на первый план выходят золотистые стафилококки, синегнойная палочка, вирусы гриппа и парагриппа. Причины постнатальных пневмоний также включают грибы рода Кандида, аденовирусы, микобактерии туберкулеза.
Основной предрасполагающий фактор пневмонии у новорожденных — недоношенность, которая в 10 раз повышает риск заболевания. На втором месте стоят дыхательные нарушения, требующие интубации и применения ИВЛ. Частота пневмоний возрастает у детей с врожденными аномалиями дыхательных путей. Легочному воспалению способствует желудочно-пищеводный рефлюкс, при котором зачастую развивается аспирационный синдром и патогенные бактерии попадают в дыхательные пути.
Патогенез
В большинстве случаев при неонатальных пневмониях наблюдается двустороннее поражение интерстициальной ткани и альвеол, которое вызывает тяжелые гипоксические расстройства и связанный с ними ацидоз. Сочетание гипоксемии и нарушений кислотно-основного равновесия провоцирует полиорганную недостаточность. В первую очередь страдает сердечно-сосудистая система, а при тяжелом течении и другие органы — почки, печень, головной мозг.
Независимо от причины, пневмонии у новорожденных протекают в 3 стадии. Сначала происходит инфильтрация (первая неделя болезни), когда поражаются преимущественно периферические отделы легких. На второй неделе начинается стадия рассасывания, характеризующаяся уменьшением процента затемненных участков и повышением пневматизации. На третьей неделе наступает этап интерстициальных изменений и деформации легочного рисунка.
Классификация
В зависимости от причины, у новорожденных выделяют бактериальную, вирусную, грибковую или протозойную формы заболевания. Если патология возникла при отсутствии других очагов инфекции в организме, ее называют первичной. Вторичное воспаление легких формируется при аспирационном синдроме, сепсисе. В современной неонатологии важна классификация пневмоний по времени развития на 2 группы:
- Врожденные. Инфицирование в этом случае происходит анте- или интранатально, а первые клинические признаки определяются в течение 3 суток после родов. Частые причины врожденного воспаления — внутриутробные инфекции.
- Приобретенные (постнатальные). Заражение патогенными микробами происходит в роддоме (нозокомиальная форма) или после выписки младенца (внебольничная форма). Симптомы выявляются спустя 72 часа после рождения ребенка, но не позже 28 дня жизни.
Симптомы пневмонии у новорожденных
У новорожденных пневмонии преимущественно проявляются неспецифическими дыхательными расстройствами. Наблюдается частое и шумное дыхание, сопровождающееся «хрюкающими звуками». При этом крылья носа раздуваются, межреберные и надключичные промежутки втягиваются. Кожа вокруг рта и на кончиках пальцев синеет, при нарастании дыхательной недостаточности отмечается тотальный цианоз.
Кашель у новорожденного обычно отсутствует. Изо рта периодически выделяется слизь или пена с неприятным запахом. Симптоматика дополняется общими признаками: отказом от сосания груди, повышением температуры тела, патологической возбудимостью или угнетением ЦНС. В неонатальном периоде пневмониям сопутствует инфекционный токсикоз, для которого характерен серый оттенок кожи, геморрагическая сыпь, желтуха и гепатоспленомегалия.
Осложнения
Болезнь может приводить к отеку легких, гнойно-деструктивным процессам (абсцессам, буллам, гангрене), пиопневмотораксу. Продолжительные дыхательные расстройства у новорожденных провоцируют гипоксическую энцефалопатию, кардиопатию, нефропатию. Наиболее тяжело протекают пневмонии у недоношенных детей: они часто заканчиваются генерализацией инфекции и сепсисом, а в 40% вызывают летальный исход.
Диагностика
Неонатолог начинает обследование со сбора анамнеза матери (течение беременности и родов, экстрагенитальные патологии), чтобы предположить причины дыхательных нарушений у новорожденного. Физикальные данные малоинформативны, поскольку у младенцев намного труднее выявить хрипы и крепитацию при аускультации. Расстройства дыхания оценивают по шкале Сильвермана или Даунса. Основными диагностическими методами для верификации возможной пневмонии у новорожденных являются:
- Рентгенография ОГК. Основной метод, который показывает очаговые или тотальные затемнения в легких, состояние плевральных синусов, наличие признаков РДС по типу «матового стекла». На снимках врач может обнаружить врожденные пороки дыхательной системы, ставшие предрасполагающим фактором заболевания.
- Микробиологическое исследование. Для установления инфекционной причины пневмонии проводят бакпосев отделяемого из зева, мокроты или трахеобронхиального аспирата. Полученные микроорганизмы исследуют на чувствительность к антибиотикам. При подозрении на сепсис выполняется посев крови на стерильность.
- Серологические реакции. Определение антител к врожденным инфекциям (цитомегаловирус, краснуха) необходимо для выяснения характера пневмонии, если типичные возбудители исключены. При визуализации на рентгенографии признаков так называемой «белой» пневмонии назначают серологические тесты на сифилис (РСК, РИБТ).
- Анализы крови. Клиническое и биохимическое исследования рекомендованы для выявления маркеров воспалительной реакции, которые соотносятся с тяжестью и прогнозом болезни. Неблагоприятным считается высокий лейкоцитарный индекс интоксикации и возрастание уровня СРБ более 10 мг/л.
Лечение пневмонии у новорожденных
Консервативная терапия
Лечение младенцев с воспалением легких проводится только стационарно: в отделении патологии новорожденных или в блоке реанимации и интенсивной терапии. Основу лечения составляют антибиотики, которые сначала подбираются эмпирически, а затем корректируются после получения результатов бактериологической диагностики. В неонатологии в основном используют бета-лактамные препараты и макролиды. Как патогенетические методы применяются:
- Кислородная поддержка. Обеспечение нормальной сатурации — первостепенная задача врачей, поскольку это снижает риск метаболических и полиорганных нарушений. Рекомендована неинвазивная вентиляция (бифазик, CIPAP), в тяжелых случаях ребенка переводят на ИВЛ.
- Иммунотерапия. Для стимуляции собственных защитных сил организма новорожденного назначают иммуноглобулины II поколения, которые включают комплекс IgG, IgM, IgA (пентаглобин).
- Инфузионная терапия. Для восполнения ОЦК и коррекции электролитных показателей показано внутривенное вливание растворов. Базовым считается 10% раствор глюкозы, который обеспечивает организм энергией. При гипоксических нарушениях эффективно ведение неотона.
Прогноз и профилактика
Вероятность полного выздоровления высокая у доношенных новорожденных без врожденных пороков и иммунодефицитов. Менее благоприятнен прогноз у недоношенных младенцев, особенно когда они требуют кислородной поддержки на ИВЛ. Профилактика неонатальных пневмоний включает антенатальную охрану плода, своевременную диагностику и лечение инфекций у беременной, предотвращение РДС путем введения дексаметазона при высоком риске преждевременных родов.
Источник
ИВЛ-ассоциированная пневмония является частым осложнением респираторной терапии у недоношенных новорожденных и фактором риска развития бронхолегочной дисплазии. В статье представлены этиологическая характеристика, основные звенья патогенеза, клиника, диагностика и терапевтические подходы Приведены данные собственного исследования перекисного окисления липидов у новорожденных на фоне респираторной терапии.
Ventilator-associated pneumonia in preterm infants
Ventilator-associated pneumonia is a common complication of respiratory therapy in preterm infants and risk factors for bronchopulmonary dysplasia. The paper presents the etiologic characteristics, the main links of pathogenesis, clinical, diagnostic and therapeutic approaches. Details of its own investigation of lipid peroxidation in infants with respiratory therapy are presented.
Проблема нозокомиальных инфекций у новорожденных в последние годы приобрела исключительно большое значение для всех стран мира в связи с их значительным ростом. Увеличение частоты внутрибольничных инфекций в значительной степени происходит за счет недоношенных новорожденных, находящихся в отделениях реанимации и интенсивной терапии, в которых концентрируются наиболее тяжелые новорожденные с респираторным дистресс синдромом. Среди внутрибольничных инфекций у новорожденных серьезную проблему в настоящее время представляют госпитальные пневмонии, развивающиеся на фоне искусственной вентиляции легких (ИВЛ), частота которых особенно высока у недоношенных детей [1, 5]. Пневмония у таких детей характеризуется распространенным характером воспаления, высокой летальностью (от 14% до 37,5%) и нередко (у 37%) она протекает с бронхообструктивным синдромом, который может быть также одним из проявлений формирующейся на фоне пневмонии хронической болезни легких — бронхолегочной дисплазии (БЛД) [2, 4, 8].
Согласно классификации, вентилятор-ассоциированные пневмонии бывают:
- Ранние — возникающие в первые 3 суток после ИВЛ;
- Поздние — формирующиеся в более отдаленные сроки.
В реализации подобной пневмонии у недоношенных детей наряду с такими факторами, как незрелость иммунитета и организма в целом, перенесенная внутриутробная гипоксия и асфиксия в родах, наличие синдромов нарушения постнатальной адаптации, большую роль играет циркуляция госпитальных штаммов микроорганизмов с повышенной устойчивостью к антибиотикам в отделениях, где концентрируются тяжелые больные. Высокий риск возникновения таких пневмоний определяется легко доступным проникновением микроорганизмов в нижние дыхательные пути через интубационную трубку, снижением факторов местной иммунной защиты дыхательных путей, механического фактора, ведущего к перерастяжению альвеол, надрыву альвеол и баротравме легкого, а также воздействию повышенной концентрации кислорода, которые могут вызвать неспецифическое воспаление. [3, 6]
Этиология. Ранние пневмонии обычно вызывают те же возбудители, что и врожденные пневмонии. Указанная особенность обусловлена, прежде всего, тем, что в их патогенезе основную роль играет микроаспирация содержимого ротоглотки и родовых путей матери. Чаще всего обнаруживают стрептококки группы В, реже — Е. coli, К. pneumoniae, S. aureus и S. Epidermidis [4]. В этиологии поздних ИВЛ-ассоциированных пневмоний у новорожденных преобладают грамотрицательные микроорганизмы (91%), среди которых превалируют энтеробактерии (69%) и псевдомонады (50%). Грамположительные возбудители нередко представлены Staphylococcus epidermidis (у 30% детей) и энтерококками (у 26%). Грибы рода Candida высеваются у 36% детей. Особенностями этиологии ИВЛ-ассоциированных пневмоний являются высокая частота ассоциаций возбудителей, их замедленная элиминация и развитие суперинфекции [3, 4].
При изучении инфекционно-воспалительных заболеваний у детей многими авторами большое значение придается патологическим процессам, происходящим на клеточном и молекулярно-генетическом уровнях, в частности процессам пероксидации [9]. Недоношенные дети имеют неразвитую систему антиоксидантной защиты и в связи с этим повышенный риск повреждения клеточных структур организма активными формами кислорода. Последние генерируются за счет использования высоких концентраций кислорода во вдыхаемой смеси при ИВЛ, но также и вследствие их образования клетками, участвующими в процессе воспаления. Результатом повреждающего действия активных форм кислорода являются инициации перекисного окисления липидов (ПОЛ). ПОЛ приводит к увеличению проницаемости липидного биослоя мембран, что обуславливает разобщение процессов окисления и фосфорилирования в митохондриях, следствием которого является энергетическое голодание клеток и их гибель. Кроме того, ПОЛ приводит к уменьшению стабильности липидного биослоя мембраны, следствием чего является развитие электрического пробоя ее собственным мембранным потенциалом и к полной потере ее барьерных свойств. [10, 11] Таким образом, основными звеньями патогенеза развития вентилятор ассоциированной пневмонии у недоношенных новорожденных являются глубокая недостаточность, как местного, так и структурного иммунитета на фоне агрессивного воздействия нозокомиальной микрофлоры и состояния оксидативного стресса, обусловленного гипероксией и инфекцией. [6, 8]
Клинической особенностью бактериальной ИВЛ — ассоциированной пневмонии у недоношенных новорожденных — является стремительное развитие заболевания и отсутствие специфических клинических симптомов, характерных только для этой патологии. Даже при развитии тяжелого воспалительного процесса в легких клинические признаки у этой категории пациентов неспецифичны, могут наблюдаться и изменяться как при инфекционных процессах (пневмония, распространенный трахеобронхит), так и при неинфекционной патологии (респираторный дистресс-синдром, аспирационный синдром, гипоксически-ишемическое поражение центральной нервной системы и другие). К ведущим клиническим симптомам относится респираторная недостаточность на фоне интоксикации. Часто это проявляется выраженной кислородозависимостью, которая увеличивает длительность аппаратной вентиляции.
Из лабораторных критериев диагностики помимо воспалительных изменений в общем анализе крови (лейкоцитоз или лейкопения, сдвиг лейкоформулы влево) используются биохимические маркеры воспаления: С-реактивный белок, прокальцитонин.
Однако у недоношенных новорожденных детей с бактериальной пневмонией уровень С-реактивного белка увеличивается не в начале заболевания, а в периоде развернутых клинических проявлений и не более чем у 60% детей. По-видимому, это связано с незрелостью организма недоношенных детей и слабой ответной реакцией на массивную бактериальную колонизацию. Более чувствительным маркером бактериальных осложнений является прокальцитонин [4, 8].
В обязательный алгоритм обследования входит рентгенография легких, однако на рентгенограммах очаговые тени выявляются лишь в 5-7%, а в остальных случаях определяется деформация легочного рисунка, снижение вентиляции легочных полей. [8, 11]. Таким образом, только совокупность клинико-лабораторных критериев позволяет обеспечить точную диагностику бактериальной пневмонии у недоношенных новорожденных детей.
Вместе с тем, ранняя и точная диагностика бактериальной пневмонии определяет своевременное и адекватное лечение заболевания, снижение летальности, развития тяжелых осложнений (сепсис, бронхолегочная дисплазия), приводящих к инвалидизации. В тоже время, помимо традиционных, нужны и новые подходы к лечению и реабилитации таких детей, что определяет актуальность разработки новых диагностических подходов [8, 13].
С целью изучения состояния оксидативного статуса у новорожденных, находящихся на искусственной вентиляции легких (ИВЛ), нами было проведено определение продуктов перекисного окисления липидов у 66 недоношенных новорожденных на фоне ИВЛ и в динамике после её завершения. Гестационный возраст наблюдаемых пациентов варьировал от 28 до 37 недель (31,59±0,34 нед.), масса тела при рождении составляла от 1120 до2380 г (2001,5±182,3 г). Анализ анамнестических данных показал, что все дети родились у женщин с отягощенным соматическим и акушерско-гинекологическим анамнезом. Хронические соматические заболевания отмечались у каждой третьей женщины (гипертоническая болезнь, бронхиальная астма, хронический бронхит, хронический пиелонефрит и др.), заболевания репродуктивных органов были диагностированы у 27 матерей (хронический аднексит, эрозия шейки матки, эндометриоз и др.). Следует подчеркнуть, что патологическое течение беременности (гестоз, анемия, угроза прерывания) отмечалось у всех женщин. Из 68 новорожденных 32 (47%) ребенка родились путем операции кесарева сечения. Оценка по шкале Апгар у 44 детей (64,7%) на 1-й минуте жизни была менее 6 баллов. Осложнения в родах в виде преждевременного отхождения околоплодных вод, кровотечения отмечались у 34 женщин (50%).
При клиническом обследовании отмечалось, что состояние всех новорожденных при рождении оценивалось как тяжелое, что потребовало проведения реанимационных мероприятия, в том числе ИВЛ в связи с наличием синдрома дыхательных расстройств (СДР). Длительность проведения ИВЛ варьировала от 3 до 16 суток. При микробиологическом исследовании содержимого интубационной трубки были выделены грамотрицательные микроорганизмы, в основном Klebsiella pneumonia, а также Pseudomonas aeruginosa, которые вместе составили 55% всех возбудителей. Грамположительные возбудители были представлены преимущественно стафилококками, среди которых преобладали гемолизирующий S.epidermidis и Enterococcusspp. (в совокупности они составляли 9%).
Показатели концентрации тиобарбитурат-реактивных продуктов у детей на ИВЛ составила 4,55±0,6 мкМ/л, а после завершения искусственной вентиляции легких — 4,95±0,45 мкМ/л. В 71,1% случаев у недоношенных детей развились респираторные осложнения ИВЛ в виде присоединения бактериальной инфекции и развития ИВЛ-ассоциированной пневмонии на поздних сроках. У них уровень ТБК составил 5,42±0,6 мкМ/л, тогда как у пациентов с более благополучным течением неонатального периода (быстрое завершение ИВЛ, короткий курс антибактериальной терапии) отмечались достоверно более низкие показатели ТБК — 4,29±0,8 мкМ/л (р<0,01). Мы полагаем, что повреждения клеточных мембран в большей степени связано с присоединением бактериальных осложнений. Это создает в последующем риск развития бронхолегочной дисплазии поскольку оксидативный стресс усугубляет повреждение легочной ткани, способствуя тем самым увеличению продолжительности и ужесточению параметров ИВЛ, вынуждает повышать концентрацию кислорода во вдыхаемой смеси, замыкая тем самым порочный круг патогенеза данного заболевания [12, 14].
ЛечениеИВЛ-ассоциированных пневмоний связано с определенными трудностями. Поскольку большинство возбудителей нозокомиальных пневмоний у недоношенных обладают высокой патогенностью и резистентностью к широкому спектру антибиотиков, антибактериальная терапия в начальном периоде должна включать комбинированное применение антибиотиков широкого спектра действия, перекрывающего спектр чувствительности всех возможных возбудителей [3, 8]. Антибактериальная терапия должна проводится под постоянным микробиологическим мониторингом для выявления резистентных госпитальных штаммов и определения их чувствительности к антимикробным препаратам. Включение иммуноглобулинов для внутривенного введения в комплекс лечения детей с респираторным дистресс-синдромом, находящихся на искусственной вентиляции легких, на 2 сутки жизни позволяет значительно снизить риск развития пневмонии, продолжительность и тяжесть заболевания. [6]. Помимо прочего в комплекс ранней реабилитации детей с ИВЛ-ассоциированной пневмонией, необходимо включать и антиоксидантную терапию.
Профилактика предусматривает целый ряд мер, направленных на улучшение качества лечения недоношенного ребенка и предупреждение экзогенной и эндогенной колонизации патогенными микроорганизмами. Необходимо, однако, указать, что не все взаимосвязи этиологии выделенной флоры, ее резистентности к антибиотикам, эффективности антибактериальной терапии и исхода заболевания в настоящее время достоверно доказаны. Поэтому накопление глубоких фундаментальных и клинических данных по проблеме вентилятор-ассоциированной пневмонии требует совместных усилий широкого круга специалистов: клиницистов, микробиологов, эпидемиологов, организаторов здравоохранения, разработчиков медицинской техники и изделий.
Е.В. Волянюк, А.И. Сафина, А.Г. Габдулхакова
Казанская государственная медицинская академия
Волянюк Елена Валерьевна — кандидат медицинских наук, ассистент кафедры педиатрии и неонатологии
Литература:
1. Рюмина И.И., Кешишян Е.С. Особенности течения синдрома дыхательных расстройств новорожденных при длительно проводимой искусственной вентиляции легких // Российский вестник перинатологии и педиатрии. — 1997. — № 3. — С. 23-28.
2. Мархулия Х.М. Этиологическая характеристика нозокомиальных пневмоний у недоношенных детей и стратегия антибактериальной терапии: автореферат дисс. … канд. мед. наук. — М., 2005. — 21 с.
3. Белобородов В.Б. Вентилятор-ассоциированная пневмония: диагностика, профилактика и лечение // Consilium medicum. — 2000. — Т. 2, № 4. — С. 10-17.
4. Дементьева Г.М., Кушнарева М.В., Мархулия Х.М. Этиология, клиника и современные методы лечения госпитальных пневмоний у новорожденных детей // Пособие для врачей. М., 2005. — 22 с.
5 Володин Н.Н. Касихина. Актуальность проблемы нозокомиальных инфекций в неонатологии // Вопросы гинекологии, акушерства и перинатологии. — 2004. — № 1. — С. 74-79.
6. Ветрова Е.В. Нарушения местного иммунитета дыхательных путей и их коррекция у недоношенных новорожденных детей с респираторным дистресс-синдромом: автореферат дисс. … канд. мед. наук. — М., 2007. — 27 с.
8. Овсянников Д.Ю., Комлева Н.А., Оболадзе Т.Б., Макарян О.В., Кузьменко Л.Г. Современные алгоритмы диагностики бронхолегочной дисплазии // Вопросы диагностики в педиатрии. — 2011. — № 1. — С. 12-20.
9. Cross A.R., Jones O.T.G. Enzymic mechanisms of superoxide production. Biochim. еt. biophys // Acta Bioenerg. — 1991. — Vol. 1057, № 3. — P. 281-298.
10. Groneck P., Schmale J., Soditt V. et. al. Bronchoalveolar inflammation following airway infection in preterm infants with chronic lung disease // Pediatr. Pulmonol. — 2001. — Vol. 31, № 5. — P. 331-338.
11. Vento M., Moro M., Escrig R., Arruza L., Villar G. Preterm Resuscitation With Low Oxygen Causes Les, Oxidative Stress, Inflammation, and ChronicLung Disease // Pediatrics. —2009. — Vol. 124. — 439 p.
12. Philip L.B., William E.T., Jeffrey D.M., Gow A. Plasma Biomarkers of Oxidative Stress: Relationship to Lung Disease and Inhaled Nitric Oxide Therapy in Premature Infants //Pediatrics. —2008. — Vol. 121. — 555 p.
13.WarrenD.K., Shukla S.J., Olsen M.A. et. al. Outcome and attributable cost of ventilator-associated pneumonia among intensive care unit patients in aSuburbanMedicalCenter// Crit. Care Med. — 2003. — Vol. 31, № 5. — P. 1312-1317.
14. Perez G., Merino N.M., Perez R.Mf.M. et. al. Respiratory morbidity after hospital discharge in premature infants born at <32 weeks gestation with bronchopulmonary dysplasia // An. Pediatr. — 2004. — Vol. 60, № 2. — P. 117-124.
Источник
