Подагра нарушение пуринового обмена у
Самым частым нарушением обмена пуринов является повышенное образование мочевой кислоты с развитием гиперурикемии. Особенностью является то, что растворимость солей мочевой кислоты (уратов) в плазме крови невелика и при превышении порога растворимости в плазме (около 0,7 ммоль/л) они кристаллизуются в периферических зонах с пониженной температурой.
В зависимости от длительности и тяжести гиперурикемия проявляется:
- Появление тофусов (греч. tophus – пористый камень, туф) – отложение уратных кристаллов в коже и подкожных слоях, в мелких суставах ног и рук, в сухожилиях, хрящах, костях и мышцах.
- Нефропатии в результате кристаллизации мочевой кислоты с поражением почечных канальцев и мочекаменная болезнь.
- Подагра – поражение мелких суставов.
Для диагностики нарушений используют определение концентрации мочевой кислоты в крови и моче.
Нарушения обмена пуринов
Подагра
Когда гиперурикемия принимает хронический характер, говорят о развитии подагры (греч. poclos – нога, agra – захват, дословно – “нога в капкане”).
В крови мочевая кислота находится в форме ее солей – уратов натрия. Из-за низкой растворимости ураты способны оседать в зонах с пониженной температурой, например, в мелких суставах стоп и пальцев ног. Накапливающиеся в межклеточном веществе ураты некоторое время фагоцитируются, но фагоциты не способны разрушить пуриновое кольцо. В результате это приводит к гибели самих фагоцитов, к выходу лизосомальных ферментов, активации свободнорадикального окисления и развитию острой воспалительной реакции – развивается подагрический артрит. В 50-75% случаев первым признаком заболевания является мучительная ночная боль в больших пальцах ног.
Длительное время подагру считали “болезнью гурманов”, однако затем внимание исследователей переместилось к наследственному изменению активности ферментов метаболизма пуринов:
- увеличение активности ФРДФ-синтетазы – приводит к избыточному синтезу пуринов,
- уменьшение активности гипоксантин-гуанин-фосфорибозил-трансферазы – из-за этого ФРДФ не используется для реутилизации пуриновых оснований, а участвует в первой реакции их синтеза. В результате возрастает количество разрушающихся пуринов и одновременно повышается их образование.
Оба ферментативных нарушения рецессивны и сцеплены с X-хромосомой. Подагрой страдает 0,3-1,7% взрослого населения земного шара, соотношение заболевших мужчин и женщин составляет 20 : 1.
Основы лечения
Диета – снижение поступления предшественников мочевой кислоты с пищей и уменьшение ее образования в организме. Для этого из рациона исключаются продукты, содержащих много пуриновых оснований – пиво, кофе, чай, шоколад, мясные продукты, печень, красное вино. Предпочтение отдается вегетарианской диете с количеством чистой воды не менее 2 л в сутки.
Реакция превращения аллопуринола
К лекарственным средствам лечения подагры относят аллопуринол, по структуре схожий с гипоксантином. Ксантиноксидаза окисляет аллопуринол в аллоксантин, и последний остается прочно связанным с активным центром фермента и ингибирует его. Фермент осуществляет, образно говоря, самоубийственный катализ. Как следствие, ксантин не превращается в мочевую кислоту, и поскольку гипоксантин и ксантин лучше растворимы в воде, то они более легко выводятся из организма с мочой.
Мочекаменная болезнь
Мочекаменная болезнь заключается в образовании солевых кристаллов (камней) разной природы в мочевыводящих путях. Непосредственно образование мочекислых камней составляет около 15% от всех случаев этой болезни. Мочекислые камни в мочевыводящих путях откладываются примерно у половины больных подагрой.
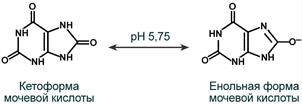
Две переходные формы мочевой кислоты при pH 5,75
Наиболее часто такие камни представлены в дистальных канальцах и собирательных трубочках. Причиной отложения кристаллов мочевой кислоты является гиперурикемия и повышенное выведение уратов натрия с мочой. Главным провоцирующим фактором кристаллизации является увеличение кислотности мочи. При понижении рН мочи ниже 5,75 ураты (енольная форма) переходят в менее растворимую кетоформу и кристаллизуются в почечных канальцах.
Закисление мочи (в норме 5,5-6,5) возникает по различным причинам. Это может быть избыточное питание мясопродуктами, содержащими большое количество нуклеиновых кислот, аминокислот и неорганических кислот, что делает такую пищу “кислой” и снижает рН мочи. Также кислотность мочи усиливается при ацидозах различного происхождения (Кислотно-основное состояние).
Кристаллы в почках могут иметь различную природу: 70-75% больных мочекаменной болезнью имеют камни щавелевой кислоты (оксалаты), 15% – мочевой кислоты, 10% – кальций-фосфатные, карбонатные, цистиновые камни. Самый большой почечный камень был извлечен 29.12.1952 из почки 80-летней женщины в Лондоне. Камень весил 6 кг 294 г.
Основы лечения
Так же, как при подагре, лечение сводится к беспуриновой диете и использованию аллопуринола. В дополнение рекомендуется растительная диета, приводящая к защелачиванию мочи, что увеличивает в моче долю более растворимой в воде енольной формы мочевой кислоты. Вместе с этим, уже имеющиеся кристаллы мочевой кислоты (а также кристаллы оксалатов) способны растворяться при подщелачивании мочи.
Лекарственное лечение непременно должно сопровождаться соблюдением беспуриновой диеты с большим количеством чистой воды, в противном случае неизбежно появление ксантиновых кристаллов в тканях и ксантиновых камней в почках.
Синдром Леша-Нихана
Болезнь Леша-Нихана (частота 1:300000) – это полное врожденное отсутствие активности гипоксантин-гуанин-фосфорибозил-трансферазы, фермента, отвечающего за реутилизацию пуриновых оснований. Признак рецессивный и сцеплен с Х-хромосомой. Впервые его описали в 1964 г в США студент-медик Майкл Леш и педиатр Уильям Нихан.
Дети рождаются клинически нормальными, только к 4-6 месяцу обнаруживаются отклонения в развитии, а именно – отставание физического развития (с трудом держит голову), повышенная возбудимость, рвота, периодическое повышение температуры. Выделение мочевой кислоты можно обнаружить еще раньше по оранжевой окраске пеленок. К концу первого года жизни симптомы нарастают, развивается нарушение координации движений, хореоатетоз, корковый паралич, спазм мышц ног. Наиболее характерный признак заболевания проявляется на 2-3-м году жизни – аутоагрессия или самокалечение – неодолимое стремление детей кусать себе губы, язык, суставы пальцев на руках и ногах. Агрессия больных распространяется также на неживые предметы и окружающих людей. Нарушения интеллекта выражены, его снижение может быть до IQ≈60.
Лечение основано на беспуриновой диете с большим количеством чистой воды и с использованием аллопуринола. Производится контроль деятельности пациента с помощью физических ограничений и психологической терапии.
Источник
Наряду с прочими патологиями, нарушение пуринового обмена тоже считается серьезным заболеванием, лечению которого следует уделить внимание. Прежде всего это сбои в метаболизме полезных веществ, которые провоцируют возникновение других болезней, например подагры, нефропатии или почечной недостаточности.
Как правило, возникает нарушение пуринового обмена у детей, но и взрослые люди тоже подвержены этой патологии. Только обычно пациенты в зрелом возрасте сталкиваются с целым рядом сопутствующих заболеваний и осложнений.
Общие сведения
Нарушение пуринового обмена по МКБ-10 имеет код Е79. Обычно это заболевание обладает хроническим характером и напрямую связано с отложением кислотных солей в тканях почек и суставах. Симптомы нарушений пуринового обмена довольно-таки специфичны и проявляются в качестве повторяющихся обострений артрита, сопровождающихся болевым синдромом.

Невыявленная и невылеченная вовремя проблема способна привести к более серьезным последствиям: например, зарождению мочекаменного заболевания и почечной недостаточности. Все терапевтические мероприятия в такой ситуации нацелены обычно на купирование неприятной симптоматики, понижение выраженности клинической картины, предотвращение развития осложнений и нормализацию метаболизма полезных веществ.
Причины патологии
Предпосылкой к развитию заболевания служит избыточное формирование пуриновых оснований либо слишком медленное их выведение с мочевой кислотой.
Первичная форма патологии объясняется наследственной предрасположенностью. А вот вторичный тип болезни может быть связан с регулярным приемом мочегонных препаратов, противовоспалительных средств и прочих медикаментов.
Нарушения пуринового обмена веществ провоцируют:
- спиртные напитки;
- сильные переохлаждения;
- некоторые фармацевтические средства;
- продукты, содержащие соответствующие образования;
- патологии инфекционного характера;
- психоэмоциональные и физические перенапряжения.

Симптомы
Признаки нарушений пуринового обмена напоминают типичные проявления сбоев метаболизма. Патологии характерен повышенный уровень креатининкиназы, который появляется практически у всех пациентов. Прочие неспецифические признаки недуга можно выявить при помощи электромиографического обследования.
У больных, имеющих нарушения пуринового обмена веществ, наблюдается чрезвычайно низкое производство аммиака, за счет чего существенно понижается работоспособность и практически полностью отсутствует аппетит. Пациенты чувствуют общее недомогание, вялость, подавленность. В некоторых случаях развивается ярко выраженная слабость.

Дети, продолжительное время страдающие от нарушений пуринового обмена веществ, зачастую остаются недоразвитыми в психическом плане и обладают повышенной склонностью к аутизму. В более редких случаях у маленьких и взрослых пациентов возникают припадки, напоминающие эпилептические, а также судороги. Кроме всего прочего, психомоторное развитие больного человека замедляется или вовсе останавливается.
Особенности
К наиболее ярким нарушениям пуринового обмена следует отнести избыточное формирование и дальнейшее накопление мочевой кислоты, которое наблюдается при подагре и синдроме Леша-Найхана. Последний кроется в наследственной нехватке определенного фермента, что приводит к неиспользованию повторно освободившихся пуринов. Вследствие чего они окисляются, преобразовываясь в мочевую кислоту.
Диагностика
Выявление заболевания чрезвычайно затруднительно и не всегда дает точный результат, поскольку эта патология обладает множеством признаков, схожих с другими нарушениями в гомеостазе. Однако при продолжительном наблюдении за состоянием пациента и его анализами в общих чертах, вполне реально обнаружить сбои в пуриновом обмене веществ и причины его появления.
Диагноз может быть поставлен на основании, прежде всего, полного отсутствия показателей функционирования почечных ферментов, активных веществ печени и скелетных мышц. При помощи лабораторных исследований частичную недостаточность можно выявить в лимфоцитах и фибробластах.

Специальное лечение, которое было бы направлено на устранение дисфункции ферментов, еще не разработано, поэтому полагаться можно только на комплексную терапию.
Лечение
Нарушения пуринового обмена требуют комплексного лечения, которое основывается прежде всего на строгой диете, включающей продукты с низким содержанием мочевой кислоты, и медикаментозной терапии.
Фармакологические методики включают несколько этапов:
- сбалансированность и нормализация обменных процессов с помощью витаминизации;
- установление метаболического ацидоза и контроль кислотной среды в моче;
- установление и постоянное поддержание нормального уровня гиперлипидемии;
- контроль и нормализация АД больного в течение суток;
- терапия вероятных осложнений патологии.
Лечение последствий
Подагра – нарушение пуринового обмена, которое не было вовремя диагностировано и вылечено. Эти заболевания очень тесно связаны между собой. Именно поэтому признаки и лечение подагры мало чем отличаются от таковых при сбоях в метаболизме. Вообще, лечение этой патологии сводится как раз к коррекции пуринового обмена. Для этого пациенту рекомендуется:
- ограничивать физическую активность в моменты обострений;
- соблюдение определенной диеты;
- питьевой режим, включающий 2 литра воды ежедневно;
- использование местных компрессов с использованием “Димексида”;
- употребление назначенных доз нестероидных противовоспалительных препаратов.
Лечение нарушения пуринового обмена может осуществляться как в стационарных условиях, так и дома. Однако последний вариант допустим исключительно после консультации со специалистом и подтверждения диагноза.
Медикаментозная терапия
Базовое лечение основывается на продолжительном употреблении препаратов, нормализующих количество мочевой кислоты в крови. Использовать медикаменты можно только в период ремиссии. В зависимости от оказываемого влияния, существует несколько разновидностей рекомендуемых препаратов:
- средства, которые уменьшают производство мочевой кислоты, к примеру, “Аллопуринол”;
- медикаменты, содержащие этебенецид, – повышают скорость выведения из организма мочевой кислоты;
- лекарства смешанного действия.
Продолжительная медикаментозная терапия целесообразна при частых атаках, выраженной клинической картине заболевания, формировании тофусов и травмировании почек.

В промежутки ремиссии пациентам также показаны разнообразные физиотерапевтические процедуры: массаж, парафиновые аппликации, ультразвук.
Диета при нарушении пуринового обмена
Практически во всех схемах лечения патологии врачи упоминают соблюдение определенного рациона. Специальная диета помогает пациенту эффективно устранить негативные последствия нарушения обмена веществ. Обычно в роли первых осложнений, с которыми действенно справляется сбалансированный рацион, выступает разлад в жировом метаболизме. На фоне этой патологии пациент стремительно набирает массу, а иногда сталкивается с атеросклерозом, ишемической болезнью сердца, а также устойчивым повышением артериального давления.
Во всех описанных ситуациях специалисты назначают пациентам диеты, в которых ограничивается количество либо полностью отсутствуют продукты, богатые пуринами. К таковым относятся: грибы, мясо, бобовые, рыба. Кроме того, больным показаны разгрузочные дни с овощным, молочным либо фруктовым меню.
Стоит сказать, что диета при нарушениях пуринового обмена должна использоваться довольно-таки долгий срок. Рацион пациента предусматривает дробное питание по 4-5 раз в течения дня.

Меню исключает продукты, содержащие щавелевую кислоту и пурины, обладает определенными ограничениями, касающимися соли, белков, жиров и углеводов. Энергетическая ценность дневного рациона должна колебаться в пределах 2700-2800 калорий. Суточное меню предусматривает потребление 80 г белков, 90 г жиров, 400 г углеводов.
Рекомендованные продукты:
- нежирные сорта мяса и рыбы;
- молочные компоненты;
- хлеб из первого сорта муки;
- всевозможные крупы;
- овощи и фрукты в любом виде.
Исключить следует:
- жирные виды рыбы и мяса;
- малину;
- крепкий чай и кофе;
- шоколад;
- какао-порошок;
- бобовые;
- клюкву;
- щавель.
Запрещены также разнообразные кулинарные жиры.
При соблюдении правильно подобранной диеты и других составляющих комплексного лечения, пациент чувствует существенное облегчение всего через несколько недель.
Источник
Понятие «подагрическая нефропатия» включает различные формы поражения почек, вызванные нарушениями пуринового обмена и другими метаболическими и сосудистыми изменениями, свойственными подагре. Подагрой страдает 1–2% населения, преимущественно мужчины [1]. Если ранние бессимптомные нарушения пуринового обмена потенциально обратимы при условии своевременной диагностики и коррекции, то на стадии тофусной подагры с поражением сосудов и органов-мишеней (сердца, мозга, почек) прогноз заболевания неблагоприятен. Поражение почек развивается у 30–50% больных подагрой. При стойком повышении уровня мочевой кислоты крови > 8 мг/дл риск последующего развития хронической почечной недостаточности (ХПН) возрастает в 3–10 раз. У каждого 4-го больного подагрой развивается ХПН [2].

В развитии подагры играют роль как приобретенные, так и наследственные факторы. Особенно велика роль неправильного питания в сочетании с гиподинамией. За последние 20 лет в Европе и США наблюдается многократный рост заболеваемости подагрой параллельно с эпидемией морбидного ожирения, нефролитиаза и инсулиннезависимого сахарного диабета [1, 3]. Особенно часто развивается подагра в странах с высоким потреблением мясных продуктов на душу населения.
Cвойственные подагре метаболический синдром с резистентностью к инсулину, а также гиперфосфатемия способствуют образованию тяжелого атеросклероза почечных и коронарных артерий с развитием ишемической болезни сердца, реноваскулярной гипертонии, присоединению к уратному кальциевого нефролитиаза.
Ведущие патогенетические механизмы подагрической нефропатии связаны с повышением синтеза мочевой кислоты в организме, а также с развитием дисбаланса между процессами канальцевой секреции и реабсорбции уратов. Гиперпродукция мочевой кислоты вызвана дефицитом гипоксантин-гуанинфосфорибозилтрансферазы (ГГФТ). ГГФТ контролируется генами, локализованными в Х-хромосоме. Этим объясняется тот факт, что подагрой заболевают почти исключительно лица мужского пола. Полный дефицит ГГФТ приводит к синдрому Леша–Найхена, характеризующемуся ранним и особенно тяжелым течением подагры. Среди других вариантов ювенильной наследственной подагры — формы, вызванные мутацией канальцевого белка Тамма–Хорсфолла, нуклеарного печеночного фактора — RCAD (renal cyst and diabetes)-синдром (сочетание подагры с кистозной дисплазией почек и инсулиннезависимым сахарным диабетом) [4]. К гиперурикемии приводит также усиленное внутриклеточное разрушение аденозинтрифосфата (АТФ): дефект, свойственный гликогенозу (I, III, V типа), врожденной непереносимости фруктозы, хроническому алкоголизму [1]. В то же время у большинства больных первичной подагрой выявляются нарушения тубулярной функции почек: снижение секреции, усиление различных фаз реабсорбции. Важную роль в патогенезе играет cпособствующий кристаллизации уратов в моче дефект канальцевого ацидогенеза [2]. Дефект проявляется образованием при подагре мочи со стойко кислой реакцией (рН < 5).
Повреждающее почки действие гиперурикозурии приводит к уратному нефролитиазу с вторичным пиелонефритом, поражению уратами интерстициальной ткани почек с развитием хронического тубуло-интерстициального нефрита, а также к ренальной острой почечной недостаточности (ОПН) за счет внутриканальцевой обструкции кристаллами мочевой кислоты (острой мочекислой нефропатии).
Гиперурикемия за счет активации почечной ренинангиотензиновой системы и циклооксигеназы-2 усиливает продукцию ренина, тромбоксана и фактора пролиферации гладкомышечных клеток сосудов, а также индуцирует атерогенную модификацию липопротеинов очень низкой плотности (ЛПОНП).
В результате развивается афферентная артериолопатия с почечной гипертонией и последующим гломерулосклерозом и нефроангиосклерозом [5].
Уратный нефролитиаз. Характеризуется, как правило, двусторонним поражением, частыми рецидивами камнеобразования, иногда коралловидным нефролитиазом. Уратные камни рентгенонегативны, лучше визуализируются на эхографии. Вне приступа изменения в анализах мочи могут отсутствовать. Почечная колика сопровождается гематурией, уратной кристаллурией. При затянувшейся почечной колике нефролитиаз может осложниться атакой вторичного пиелонефрита, постренальной ОПН. При длительном течении приводит к гидронефротической трансформации почки, пионефрозу.
Хронический тубулоинтерстициальный нефрит. Проявляется стойким мочевым синдромом, часто сочетающимся с артериальной гипертонией. При этом протеинурия, не превышающая 2 г/л более чем у половины больных, сочетается с микрогематурией. Конкрементов обычно не обнаруживается, однако отмечаются эпизоды макрогематурии с преходящей олигурией и азотемией, провоцируемые дегидратацией. У 1/3 больных обнаруживаются двусторонние медуллярные кисты (0,5–3 cм в диаметре). Типично раннее присоединение гипостенурии и никтурии, а также гипертонии с гломерулосклерозом. Артериальная гипертония обычно носит контролируемый характер. Появление трудноконтролируемой гипертонии свидетельствует о прогрессировании гломерулосклероза и нефроангиосклероза или формировании атеросклеротического стеноза почечных артерий.
Острая мочекислая нефропатия. Манифестирует внезапно олигурией, тупыми болями в пояснице с дизурией и макрогематурией, нередко сочетающимися с атакой подагрического артрита, гипертоническим кризом, приступом почечной колики. Олигурия сопровождается выделением мочи красно-бурого цвета (уратная кристаллурия). При этом концентрационная способность почек относительно сохранна, экскреция натрия с мочой не увеличена.
В дальнейшем олигурия быстро переходит в анурию. При усугублении внутриканальцевой обструкции образованием многочисленных уратных конкрементов в мочевых путях и в мочевом пузыре азотемия нарастает особенно высокими темпами, что позволяет отнести этот вариант к ургентной форме внезапно наступающей подагрической нефропатии.
Диагноз и дифференциальная диагностика
Клинически диагноз подагры наиболее вероятен при pазвитии острого артрита на фоне проявлений метаболического синдрома — алиментарного ожирения абдоминального типа в сочетании с объем-натрийзависимой гипертонией, гиперлипидемией, гиперинсулинемией, микроальбуминурией. Лабораторная диагностика подагры основывается на выявлении нарушений обмена мочевой кислоты: обнаружении гиперурикемии (> 7 мг/дл), гиперурикозурии (> 1100 мг/сут ), стойко кислой рН мочи, протеинурии (микроальбуминурии), гематурии, кристаллурии. Инструментальная диагностика включает ультразвуковое исследование (идентификация рентгенонегативных уратных конкрементов), а также (в сложных случаях) биопсию пораженного сустава, тофуса. При этом информативно обнаружение внутриклеточных кристаллов мочевой кислоты в синовиальной жидкости и в содержимом тофусов (методом поляризационной микроскопии). Ультразвуковая допплерография проводится при трудноконтролируемой гипертонии у больных подагрой с целью исключения атеросклеротического стеноза почечных артерий.
Вторым этапом диагностики является разграничение подагры и вторичных гиперурикемий. Среди заболеваний, часто сопровождающихся нарушениями пуринового обмена, известны: хроническая свинцовая интоксикация (свинцовая нефропатия), хроническое злоупотребление алкоголем, анальгетическая нефропатия, распространенный псориаз, саркоидоз, бериллиоз, гипотиреоз, миелопролиферативные заболевания, поликистозная болезнь, цистиноз. Гиперурикемия при алкоголизме, как правило, протекает бессимптомно и характеризуется эксцессзависимостью [6]. Следует подчеркнуть неблагоприятное прогностическое значение гиперурикемии при нефропатии беременных [7], при иммуноглобулин А (IgA)-нефропатии [8] и при алкоголизме [6]. Большую опасность представляет синдром лизиса опухоли: острая мочекислая нефропатия, осложняющая химиотерапию онкологических заболеваний. Для хронического тубулоинтерстициального нефрита характерны гипертония, ранняя анемия, остеопороз. Нередок исход в ХПН. Диагностика основывается на обнаружении повышенной концентрации свинца в крови и моче после пробы с комплексонами (ЕДТА — от англ. этилендиаминтетрауксусная кислота) [9]. Индуцированную лекарствами вторичную гиперурикемию также необходимо дифференцировать с первичной подагрой. К лекарственным средствам, вызывающим гиперурикемию, относятся: тиазидные и (в меньшей степени) петлевые диуретики, салицилаты, нестероидные противовоспалительные препараты, никотиновая кислота, этамбутол, циклоспорин, противоопухолевые цитостатики и антибиотики, рибавирин. Особенно важна диагностика ХПН (подагрической «маски» уремии), резко нарушающей почечную элиминацию мочевой кислоты [2].
Течение и прогноз подагрической нефропатии
Подагрическая нефропатия обычно возникает на одном из этапов многолетнего течения хронической «тофусной» подагры с атаками подагрического артрита. В то же время в 30–40% случаев нефропатия является первым проявлением — почечной «маской» — подагры или развивается на фоне атипичного для подагры суставного синдрома (поражение крупных суставов, полиартрит, артралгии).
О далеко зашедшей подагре с риском поражения органов-мишеней свидетельствуют гипертония с нарушением циркадного ритма, формирование метаболического синдрома, микроальбуминурия, значительное повышение липидов (холестерин липопротеинов низкой плотности > 130 мг% ), C-реактивного белка. Cреди ранних признаков поражения органов-мишеней при подагре: стойкая протеинурия, умеренное снижение клубочковой фильтрации (до 60–80 мл/мин), гипертрофия левого желудочка, присоединение сахарного диабета. Для подагрической нефропатии типично латентное или рецидивирующее течение с двусторонними почечными коликами (уратный нефролитиаз), повторными эпизодами обратимой ренальной ОПН (острая мочекислая нефропатия). От клинической манифестации подагрической нефропатии до появления ХПН в среднем проходит 12 лет.
К факторам риска развития ХПН при подагре относятся — стойкая артериальная гипертония, протеинурия > 1 г/л, присоединение хронического пиелонефрита, сахарный диабет, старческий возраст больного подагрой, ювенильные формы подагры, хронический алкоголизм.
Лечение подагрической нефропатии
Лечение острой мочекислой нефропатии проводится в соответствии с принципами лечения ОПН, вызванной острой внутриканальцевой обструкцией. При отсутствии анурии, признаков обструкции мочеточников уратами (постренальной ОПН ) или двустороннего атеросклеротического стеноза почечных артерий (ишемической болезни почек) применяется консервативное лечение. Используется непрерывная интенсивная инфузионная терапия ( 400–600 мл/ч) с применением изотонического раствора хлорида натрия, 4% раствора гидрокарбоната натрия и 5% глюкозы, 10% раствора маннитола (3–5 мл/кг/ч), фуросемида (до 1,5–2 г/сут, дробными дозами). При этом диурез должен поддерживаться на уровне 100–200 мл/ч, а рН мочи достигать значения 6,5, что обеспечивает растворение уратов и выведение мочевой кислоты. Одновременно назначается аллопуринол в дозе 8 мг/кг/сут или уратоксидаза (0,2 мг/кг/сут, внутривенно). При отсутствии эффекта от указанной терапии в течение 60 ч больного переводят на острый гемодиализ. В том случае, если острая мочекислая нефропатия развилась как осложнение химиотерапии опухоли (гемобластоза) в рамках вторичной гиперурикемии — при синдроме лизиса опухоли, cразу показан экстренный гемодиализ (гемодиафильтрация) вместе с аллопуринолом в виду низкой эффективности консервативной инфузионной терапии.
Лечение хронических форм подагрической нефропатии должно быть комплексным и предусматривать решение следующих задач:
- коррекция нарушений пуринового обмена;
- коррекция метаболического ацидоза и рН мочи;
- нормализация величины и суточного (циркадного) ритма артериального давления (АД);
- коррекция гиперлипидемии и гиперфосфатемии;
- лечение осложнений (в первую очередь хронического пиелонефрита).
Диета должна быть малопуриновой, низкокалорийной и сочетаться с обильным щелочным питьем (2–3 л/сут). Суточная квота белков не должна превышать 1 г/кг, жиров — 1 г/кг. Длительное соблюдение такой диеты снижает уровень мочевой кислоты крови на 10% (урикозурию — на 200–400 мг/сут), способствует нормализации массы тела, липидов и фосфатов крови, а также уменьшению метаболического ацидоза. Целесообразно обогащение диеты цитратом калия или бикарбонатом калия, а также рыбьим жиром. Эйкозапентаеновая кислота — действующее начало рыбьего жира — за счет высокого содержания полиненасыщенных жирных кислот оказывает при подагре нефропротективное и кардиопротективное действие. Ее длительное применение уменьшает объем жировой ткани, протеинурию, инсулинорезистентность, дислипидемию, гипертонию. При подагрической нефропатии в стадии ХПН должна использоваться малобелковая диета (0,6–0,8 г/кг).
Перечислим препараты, влияющие на пуриновый обмен.
- Купирующие подагрический артрит: колхицин; нестероидные противовоспалительные препараты; глюкокортикостероиды.
- Ингибиторы ксантиноксидазы: аллопуринол (милурит); уратоксидаза (расбуриказа).
- Урикозурические препараты: бензбромарон, сульфинпиразон, пробенецид; блокаторы рецепторов ангиотензина II (А II); статины.
- Цитратные смеси: уралит; магурлит; лемарен.
К препаратам, контролирующим гипертонию при подагре, относятся:
- ингибиторы ангиотензинпревращающего фермента (АПФ);
- блокаторы рецепторов А II;
- антагонисты кальция;
- селективные β-адреноблокаторы;
- петлевые диуретики;
- статины;
- фибраты.
Аллопуринол (милурит) cнижает продукцию и уровень мочевой кислоты крови, ингибируя фермент кcантиноксидазу. Способствует растворению уратов. Гипоурикемическое действие аллопуринола коррелирует с его нефропротективным эффектом, связанным со снижением протеинурии, продукции ренина, свободных радикалов, а также с замедлением гломерулосклероза и нефроангиосклероза. Показания к применению аллопуринола: бессимптомная гиперурикемия в сочетании с гиперурикозурией > 1100 мг/сут, подагрический хронический тубулоинтерстициальный нефрит, уратный нефролитиаз, профилактика острой мочекислой нефропатии у онкологических больных и ее лечение.
Суточная доза аллопуринола (от 200 до 600 мг/сут) зависит от выраженности гиперурикемии. В виду возможности обострения подагрического артрита целесообразно начинать лечение аллопуринолом в стационаре и в течение 7–10 дней комбинировать препарат с нестероидными противовоспалительными препаратами или колхицином (1,5 мг/сут). В первые недели лечения уратного нефролитиаза аллопуринолом желательно cочетать его с препаратами, повышающими растворимость уратов в моче (магурлит, уралит, бикарбонат калия, диакарб). При хроническом тубуло-интерстициальном нефрите дозу аллопуринола уменьшают по мере снижения клубочковой фильтрации, а при выраженной ХПН (креатинин сыворотки > 500 мкмоль/л) он противопоказан. Аллопуринол усиливает эффект непрямых антикоагулянтов и усугубляет токсическое действие азатиоприна на костный мозг. При обнаружении гиперурикемии (подагры) у реципиента после трансплантации необходимо снижение дозы циклоспорина и салуретиков. При отсутствии эффекта заменяют азатиоприн на микофенолат мофетил и только после этого присоединяют аллопуринол [10].
Урикозурические препараты корригируют гиперурикемию путем увеличения экскреции мочевой кислоты с мочой. Применяются при бессимптомной гиперурикемии, подагрическом хроническом тубулоинтерстициальном нефрите. Противопоказаны при гиперурикозурии, при уратном нефролитиазе, при ХПН. Чаще применяются пробенецид (начальная доза 0,5 г/сут), cульфинпиразон (0,1 г/сут), бензобромарон (0,1 г/сут). Возможна комбинация аллопуринола с бензобромароном или сульфинпиразоном. Урикозурическим эффектом обладает также лозартан и другие блокаторы рецепторов-II.
Цитратные смеси (уралит, магурлит, блемарен) корригируют метаболический ацидоз, повышают рН мочи до 6,5–7 и за счет этого растворяют мелкие уратные конкременты. Показаны при уратном нефролитиазе. Уралит или магурлит принимают до еды 3–4 раза в сутки в суточной дозе 6–10 г. При лечении необходим постоянный контроль за рН мочи, так как ее резкое ощелачивание может привести к кристаллизации фосфатов. Цитратные смеси противопоказаны при ХПН, при активном пиелонефрите, должны с осторожностью применяться при гипертонии (содержат много натрия). Цитратные смеси не эффективны при крупных конкрементах, когда показана дистанционная литотрипсия или пиелолитотомия.
В задачи гипотензивной терапии при подагрической нефропатии входит обеспечение нефропротективного и кардиопротективного эффектов. Не должны использоваться препараты, задерживающие мочевую кислоту (тиазидные диуретики), усугубляющие гиперлипидемию (неселективные β-адреноблокаторы). Препаратами выбора являются ингибиторы АПФ, блокаторы рецепторов А II, антагонисты кальция, селективные β-адреноблокаторы.
Статины (ловастатин, флувастатин, правастатин) применяются у больных подагрой с уровнем холестерина липопротеинов низкой плотности > 130 мг%. Статины III поколения (аторвастатин) обладают независимым гипоурикемическим эффектом [11].
Наиболее эффективна при подагрической нефропатии комбинация ингибиторов АПФ с блокаторами рецепторов A II, статинами и аллопуринолом. При указанном сочетании усиливаются гипоурикемический, антипротеинурический, гиполипидемический и гипотензивный эффекты c восстановлением циркадного ритма АД и замедлением ремоделирования миокарда левого желудочка, снижается риск формирования метаболического синдрома и сахарного диабета, уменьшается концентрации в крови С-реактивного белка. В результате снижается риск развития острого инфаркта миокарда, острых нарушений мозгового кровообращения и исхода в ХПН.
Литература
- Бунчук Н. В. Подагра// Ревматические болезни/ под ред. В. А. Насоновой и Н. В. Бунчука. М., 1997. C. 363–374.
- Mухин Н. А., Балкаров И. М. Подагрическая почка// Нефрология/ под ред. И. Е. Тареевой. M., 2000. C. 422–429.
- Stamatelou K. K. , Francis M. E., Jones C. A. Time trends is reported prevalence of kidney stones in the U.S.// Kidney Int. 2003; 63: 1817–1823.
- Bingham C., Ellard S. et al. Atypical familial juvenile hyperuricemic nephropathy associated with a hepatocyte nuclear factor-1 beta gene mutation // Kidney Int. 2003; 63: 1645–1651.
- Kang D. H., Nakagawa T., Feng L. A Role of uric acid in progression of renal disease // J. Amer. Soc. Nephrol. 2002; 13: 2888–2897.
- Николаев А. Ю. Нарушения пуринового обмена при алкоголизме// Алкогольная болезнь/ под ред. В. С. Моисеева. M., 1990. C. 95–99.
- Karumanchi S. A., Maynard S. E., Stillman I. E. Preeclampsia: a renal perspective// Kidney Int. 2005; 67: 2101–2113.
- Ohno T., Hosoya T., Gomi H. Serum uric acid and renal prognosis in IgA-nephropathy // Nephron — 2001; 87: 333–339.
- Munter P., He J., Vupputuri S. Blood lead and CKD in the general US population: results from NHANES III. Kidney Int. 2003; 63: 1044–1050.
- Perez-Ruiz F., Gomez-Ullate P., Amenabar J. Long-term efficiacy of hyperuricaemia treatment of renal transplant patients // Nephrol. Dial. Transpl. 2003; 18: 603–606.
- Athyros V. G., Elisaf M., Papageorgiou A. A. Effect of statins versus untreated dyslipidemia on s
