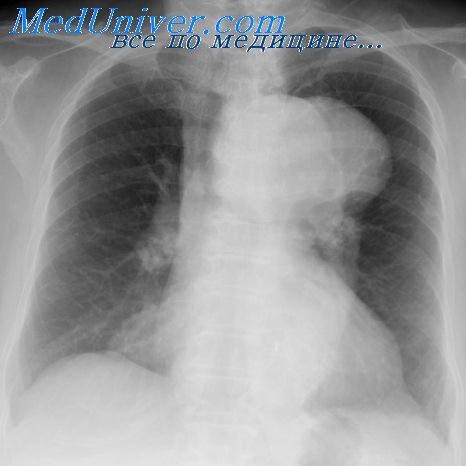
Пневмония у детей с пороком сердца
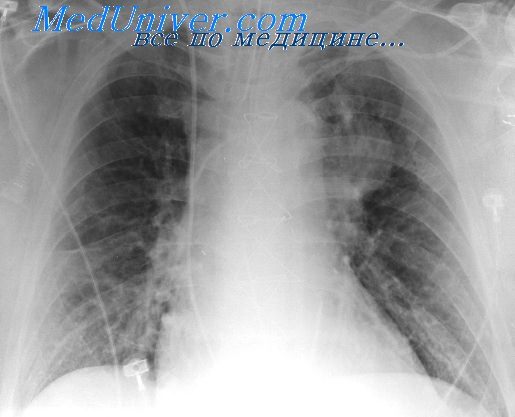
Болезни легких у детей с пороком сердца. Частота повторных пневмоний при ВПСИзучение повторных заболеваний органов дыхания у больных врожденными пороками сердца имеет важное значение, так как заболевания легких значительно отягощают их течение. До настоящего времени имеется лишь небольшое количество работ, указывающих на значение заболеваний органов дыхания в клинике врожденных пороков сердца. Во многих отечественных и зарубежных руководствах по кардиологии о сопутствующих заболеваниях органов дыхания сказано вскользь или вообще не упоминается. Исключением является работа К. Ф. Ширяевой (1965), посвященная изучению клинического течения врожденных пороков сердца. Автор наблюдала пневмонии у 93% детей, страдающих врожденными пороками сердца. Повторные пневмонии и переход их в хронические она часто отмечала в раннем детском возрасте. Известно, что пневмонии у больных врожденными пороками сердца, особенно в раннем детском возрасте, могут привести к летальному исходу или явиться причиной сердечной недостаточности. Среди больных, страдающих хронической пневмонией, по данным М. Г. Чукловиной (1961, 1962, 1963), 12,4% составляют дети, страдающие врожденными пороками сердца. При анализе материала Института хирургии им. А. В. Вишневского мы пытались установить не только частоту повторных пневмоний при различных врожденных пороках сердца, но и зависимость их от легочной гемодинамики, влияние на течение врожденных пороков сердца, развитие легочной гипертензии при них. Многие исследователи, изучавшие клинику врожденных пороков сердца с лево-правым сбросом, указывают, что в анамнезе у больных, страдающих этими пороками, отмечены многократные пневмонии (Metniani, 1954; Downing, Goldberc, 1956; М. С. Маслов, 1958; А. А. Кешишева, 1958; Gall, Cooleg, 1961; Ф. X, Кутушев, 1962; К. Ф. Ширяева, 1962, 1965).
Следует отметить, что еще Roger в 1879 г. подчеркивал, что больные, страдающие дефектом межжелудочковой перегородки, могут быть подвержены простудным заболеваниям. Maxwell (1957) отмечал, что «респираторные» инфекции характерны для больных как с левоправым, так и с право-левым шунтом. Проводя анализ частоты этих осложнений и влияния их на гемодинамику, он не указывал, какие респираторные инфекции имеет в виду: катары верхних дыхательных путей, повторные бронхиты или пневмонии. По его данным, для обеих групп больных характерны частые респираторные инфекции — 54% для больных тетрадой Фалло, 59—69% для больных с лево-правым сбросом. Исключение составляют больные с открытым артериальным протоком и дефектом межжелудочковой перегородки в стадии легочной гипертензии. У этих больных он не наблюдал респираторных инфекций. Частота повторных пневмоний при открытом артериальном протоке, по литературным данным, ко.леблется. Воr, Samanek (I960) отметили повторные пневмонии и бронхиты у 39% обследованных больных. Helsingen, Huson, Efsking (1958)—у 23% оперированных, Ф. Х. Кутушев (1959, 1962) — у 30% больных, при этом у 3 — открытый артериальный проток сочетался с бронхоэктазами. А. А. Кешишева (1958) из 46 больных, оперированных по поводу открытого артериального протока, пневмонии и бронхиты наблюдала у 41 (89%), причем у 20 — более 3 раз. О сочетании открытого артериального протока и бронхоэктатической болезни сообщают и другие авторы (B.C. Шапкин, 1955; С. А. Либов и К. Ф. Ширяева. 1955, 1962; И. К Охотин, 1960; М. Г. Чухловина, 1961). При дефекте межпредсердной перегородки также отмечены частые повторные пневмонии. Так, М. И. Бурмистров (1959) наблюдал повторные пневмонии у 20 из 38 больных, Dawning, Goldberg (1956) —у 26 из 100, Smuhl, Lamb (1952) —у 5 из 15, Swan с соавторами (1959) —у 31 из 100, Maxwell — у 27 из 41 больного. При- этом также возможно развитие третьей фазы хронической пневмонии — бронхоэктатической болезни (Edwards с соавт., 1955; С. Л. Либов, 1962; А. П. Колесов, Ф. X. Кутушев, 1963). Столь же часты повторные пневмонии и бронхиты при дефекте межжелудочковой перегородки. По наблюдениям С. Э. Островского (1911), из 17 детей, страдавших дефектом межжелудочковой перегородки, от пневмонии погибло 11 (65%)). Такие же данные приводит Н. И. Рагоза (1913). Dawning, Goldberg (1956) отметили повторные пневмонии у 33%, Н. С. Кухарева (1965) — у 77% больных. Заболеваниям повторными пневмониями подвержены больные с большими размерами артериовенозного шунта (Кау с соавт., 1957; С. А. Колесников и М. В. Муравьев, 1962; К. Ф. Ширяева, 1965). При врожденных пороках сердца с уменьшенным легочным кровотоком также бывают респираторные инфекции (Mason, 1955; Maxwell, 1957; Н. К. Галанкин, 1958; Crafford, 1959). – Также рекомендуем “Причины повторных пневмоний при пороке сердца. Патогенез повторных пневмоний у детей с ВПС” Оглавление темы “Нарушения ритма, пневмонии у детей с пороком сердца”: |
Источник
Причины повторных пневмоний при пороке сердца. Патогенез повторных пневмоний у детей с ВПС
При пороках сердца с неизмененным легочным кровотоком (аортальный стеноз, коарктация аорты) Maxwell (1957) совсем не наблюдал респираторных заболеваний.
Мы изучили заболеваемость повторными пневмониями у 2499 больных. В это количество не вошли больные, у которых не был уточнен характер врожденного порока сердца.
Сравнение частоты повторных пневмоний при различных врожденных пороках сердца показывает, что для всех пороков с увеличенным легочным кровотоком характерны повторные пневмонии. Из 1246 больных, страдающих пороком сердца с увеличенным легочным кровотоком, 627 (51%) перенесли пневмонии, из них 477 (39%) более 2 раз.
Больные врожденным пороком сердца с увеличенным легочным кровотоком и цианозом (транспозиция магистральных сосудов без стеноза легочной артерии) также страдают повторными заболеваниями легких. Для больных врожденными пороками сердца с уменьшенным легочным кровотоком характерны одно-двукратные пневмонии в раннем детском возрасте, повторные — у них наблюдаются значительно реже.
При пороках сердца с неизмененным легочным кровотоком повторные заболевания легких наблюдались лишь у 7 больных из 176. Этот факт еще раз указывает на значение легочной гемодинамики в развитии повторных пневмоний.
Повторные катары верхних дыхательных путей и бронхиты отмечены нами во всех группах больных независимо от легочной гемодинамики.
Повторные респираторные заболевания отмечены нами при всех врожденных пороках сердца (в среднем около 30%). Несколько реже наблюдаются повторные бронхиты.

Патогенез – механизмы развития повторных пневмоний. Ведущую роль в возникновении воспалительного процесса легких имеет состояние макроорганизма, сопротивляемость его возбудителю инфекции (В. И. Молчанов, 1932; И. В. Давыдовский, 1956; Ю. Ф. Домбровская, 1957; М. С. Маслов, 1957).
Микробная флора, являющаяся постоянным обитателем дыхательных путей здорового человека, вызывает воспалительный процесс при условии понижения сопротивляемости организма.
Известно, что у новорожденных и детей раннего возраста без врожденного порока сердца формирование бронхиального дерева еще не закончено. Деление бронхов и образование новых альвеол продолжается до 11— 13 лет (Broman, 1923; Emery, Mithal, 1960).
Наряду с недоразвитием альвеол в раннем возрасте имеет место значительное развитие соединительной ткани, обильно снабженной кровеносными и лимфатическими сосудами. Относительная широта респираторных бронхиол и ацинусов способствует легкому распространению инфекции (М. А. Скворцов, 1951).
Частота заболеваний органов дыхания у больных врожденными пороками сердца с увеличенным и уменьшенным легочным кровотоком различна.
В основе патогенеза повторных пневмоний при врожденных пороках сердца с увеличенным легочным кровотоком, по мнению большинства исследователей, лежит гиперволемия сосудов малого круга кровообращения (Taussig, 1947; М. С. Маслов, 1957; Ф. X. Кутушев, 1959; 1962), а при пороках с уменьшенным легочным кровотоком — измененная реактивность организма, сенсибилизация его (А. Н. Петрова, 1965).
Для больных, страдающих врожденными пороками сердца с увеличенным легочным кровотоком, характерным является полнокровие легких, обусловленное сбросом крови слева направо. Переполнение легочных сосудов кровью приводит к застойным явлениям в легких. Вследствие этого уменьшается эластичность легочной ткани, нарушается дренажная функция бронхов, что благоприятствует возникновению воспалительных явлений в легких. Имеет значение также низкое сосудистое сопротивление и большая емкость сосудов малого круга кровообращения. При повышении сосудистого сопротивления заболеваемость пневмониями уменьшается.
Ф. X. Кутушев у больных с незаращением артериального протока обнаружил утолщение альвеолярных мембран; в связи с этим возникают затруднения для свободного газообмена в легких с нарушением диффузного компонента внешнего дыхания. Это является предрасполагающим моментом к возникновению повторных пневмоний и затяжному их течению.
– Также рекомендуем “Хронические пневмонии у детей с пороком сердца. Легочная гипертензия и повторные пневмонии”
Оглавление темы “Нарушения ритма, пневмонии у детей с пороком сердца”:
1. Мерцательная аритмия при ВПС. Атрио-вентрикулярная блокада при пороке сердца у детей
2. Врожденная атрио-вентрикулярная блокада у детей. Приступ Морганьи—Эдемс—Стокса
3. Синдром Вольф — Паркинсон — Уайта (WPW) у детей. Аневризма легочной артерии и аорты при пороке сердца
4. Болезни легких у детей с пороком сердца. Частота повторных пневмоний при ВПС
5. Причины повторных пневмоний при пороке сердца. Патогенез повторных пневмоний у детей с ВПС
6. Хронические пневмонии у детей с пороком сердца. Легочная гипертензия и повторные пневмонии
7. Клиника повтороных пневмоний у детей. Течение повторных пневмоний при пороке сердца
8. Пример повторных пневмоний у ребенка. Хроническая пневмония при открытом артериальном протоке
9. Сочетание порока сердца и бронхоэктатической болезни. Зависимость частоты пневмоний от гипертензии в малом круге
10. Внешнее дыхание у детей при пороке сердца. Степень легочной гипертензии и хронические пневмонии
Источник
Похожие темы научных работ по медицине и здравоохранению , автор научной работы — Дегтярева Е.А., Павлова Е.С., Овсянников Д.Ю., Вавилова Г.Н.,
Е.А. Дегтярева, Е.С. Павлова, Д.Ю. Овсянников, Г.Н. Вавилова ПНЕВМОНИЯ У МЛАДЕНЦЕВ С ВРОЖДЕННЫМИ ПОРОКАМИ СЕРДЦА
ГОУ ВПО Российский университет дружбы народов, Детская инфекционная клиническая больница № 6 г. Москвы
В настоящее время прогресс кардиохирургии сделал возможным выполнение первичной радикальной коррекции врожденных пороков сердца (ВПС) у младенцев, начиная с периода новорожденности. Вместе с тем, кар-диохирургическое вмешательство нередко выполняется несвоевременно в связи с инфекциями нижних дыхательных путей (ИНДП), часто имеющих осложненное течение и высокий риск летального исхода.
Целью работы явилось изучение особенностей течения пневмонии у младенцев с ВПС в дооперационном периоде в зависимости от декомпенсации кровообращения, гиперволемии малого круга кровообращения, артериальной гипоксемии и установление факторов риска неблагоприятного исхода.
За период 2008-2010 гг. обследованы 100 младенцев в возрасте 6,6±1,75 нед (0,15-24 нед) (мальчиков — 53, девочек — 47) с ВПС, госпитализированных как из других стационаров, в том числе кардиохирургических клиник г. Москвы, так и из дома, в отделение инфекционной кардиологии ДИКБ № 6 с направляющим диагнозом пневмония на 6,4±2,1 день (1,2-40 дней) заболевания. Структура ВПС у наблюдаемых детей была следующей: бледные — у 70 детей (в большинстве случаев с артериальной гиперволемией — 66, в том числе осложненные легочной гипертензией у 2/з больных), цианотические — у 30 детей.
В ходе обследования, включавшего клинический и биохимический (с определением маркеров С-реактив-ного белка — СРБ и маркеров повреждения миокарда) анализы крови, прокальцитониновый тест, серологическую диагностику с определением IgM, IgG к M. рneu-moniae, C. рneumoniae, Р. jirovici (carinii), рентгенографию (РГК) и высокоразрешающую компьютерную томографию (ВРКТ) органов грудной клетки, у 80 детей диагноз пневмонии был подтвержден, в том числе у 10 — микоплазменной, хламидийной, пневмоцистной этиологии. У 10 детей на РГК пневмонию симулировали проявления интерстициального отека в результате декомпенсированной сердечной недостаточности с быстрой (1-3 дня) обратной динамикой на фоне
адекватной терапии недостаточности кровообращения (НК). В остальных случаях установить генез снижения пневматизации позволило проведение ВРКТ: у 5 детей выявлены множественные ателектазы, у одного
— облитерирующий бронхиолит на фоне гиперволемии малого круга кровообращения, у 2 — врожденные пороки развития легких (гипоплазия, аномалия ветвления бронхов); бронхолегочная дисплазия, туберкулез (по одному пациенту).
В зависимости от клинико-морфологической формы пневмония у детей с ВПС носила очаговый (у 20 пациентов), очагово-сливной (у 26), сегментарный (у 15), долевой (у одного ребенка), интерстициальный (у 18) характер; затяжное течение пневмония имела у 2 больных, тяжелое — у 35.
Пневмония у детей с ВПС имела клинико-лабо-раторные особенности: высокую частоту (40%) брон-хообструктивного синдрома, отсутствия фебрильной лихорадки (47%) и лейкоцитоза более 15-109/л (65%), повышения уровня СРБ (88%). У детей с пневмонией и ВПС значимое повышение маркеров повреждения миокарда (изоферменты лактатдегидрогеназы 1, 2; кре-атинфосфокиназа МВ) не сопровождалось выявлением маркера некробиолиза кардиомиоцитов тропонина, что свидетельствует в пользу инфекционно-токсического и гипоксического генеза повреждения миокарда. У 20 больных пневмония имела осложненное течение. Среди осложнений с наибольшей частотой (у 13 больных) регистрировался инфекционно-токсический шок; реже
— плеврит (у 3), полостные образования (у 4).
Летальность среди пациентов с пневмонией и ВПС составила 19%. К летальному исходу предрасполагали отсутствие своевременного кардиохирургического лечения у детей с гемодинамически значимыми сложными ВПС; синдромальная патология, сопровождающаяся иммунной недостаточностью (синдромы Дауна, Эдвардса, Ди Джоржи); тяжелая энцефалопатия любого генеза; повторная госпитализация и антибактериальная терапия в течение предшествующих данной госпитализации 3 месяцев.
Наиболее частые осложнения ВПС — Прогрессирующая дистрофия анемия, рецидивирующая пневмония, инфекционный эндокардит тромбоэмболический синдром, нарушения ритма и проводимости, легочная гипертензия, хроническая сердечная недостаточность.
1) длительный хронический бронхолегочный процесс (хроническая пневмония, хроническая обструктивная болезнь легких, хроническая эмфизема легких, бронхоэктатическая болезнь и др.), при котором пневмосклероз сопровождается запустеванием и облитерацией сосудов малого круга кровообращения;
2) длительно существующая хроническая сердечная недостаточность (митральные и аортальные пороки сердца, кардиомиопатии и др.) с длительным венозным застоем в МКК (венозная или застойная гипертензия);
3) длительное артериовенозное шунтирование крови при врожденном пороке сердца с обогащением малого круга кровообращения (гиперкинетически-гиперволемическая или артериальная прекапиллярная легочная гипертензия);
У детей, страдающих врожденным пороком сердца с обогащением малого круга кровообращения, формирование легочной гипертензии проходит три основных фазы:
1)гиперволемическую; 2)смешанную; 3) склеротическую.
Для гиперволемической фазы характерны большой артериовенозный сброс в малый круг кровообращения, гиперволемия сосудов легких, в ответ на которую возникает незначительный защитный спазм сосудов, без увеличения общелегочного сопротивления. Давление в легочной артерии остается нормальным или умеренно возрастает.
Для смешанной фазы характерно защитное повышение давления в системе легочной артерии, вызванное спазмом сосудов легких. За счет этого механизма уменьшается величина артериовенозного сброса крови при увеличении общелегочного сопротивления кровотоку.
Данная гипертензия является функциональной, т. е. обусловлена в основном гиперволемией и повышением тонуса сосудистой стенки за счет вазоконстрикции и гипертрофии средней оболочки мелких мышечных артерий. Для склеротической фазы характерны деструктивные изменения сосудистой стенки, когда на фоне гипертрофии средней оболочки мелких мышечных артерий наступает склероз внутренней оболочки с последующим истончением стенки артерий их генерализованной дилатацией и развитием некротизирующего артериита.
В склеротической фазе отмечаются высокая необратимая легочная гипертензия, расширение легочной артерии, стойкий цианоз и выраженная гипертрофия с систолической перегрузкой правых отделов сердца, часто с проявлениями хронической правожелудочковой недостаточности, т. е. с развитием вторичного комплекса Эйзенменгера.
Выделение стадий легочной гипертензии имеет чрезвычайно большое практическое значение, т.к. помогает определять тактику консервативного ведения больного, уточнить рациональные сроки оперативного вмешательства, прогнозировать результаты хирургической коррекции (процент послеоперационной летальности), характер реабилитации и качество жизни, продолжительность жизни пациентов и др.
В.И.Бураковским и соавт. (1975) создана клиническая классификация легочной гипертензии (ЛГ), основанная на показателях процентного отношения величины систолического давления в легочной артерии к величине системного артериального давления (систолическое артериальное давление легочной артерии/систолическое артериальное давление аорты, %), процентного отношения величины артериовенозного сброса крови через дефект к величине минутного объема крови М КК, процентного отношения величины общего легочного сосудистого сопротивления к величине системного периферического сопротивления (см. таблицу).
Таблица 2 Классификация легочной гипертензии
Отношение систолического давления в легочном стволе к системному артериальному давлению, %
Сброс крови по отношению к минутному объему кровообращения в малом кругу кровообращения, %
Отношение общего легочного сосудистого сопротивления к системному. %
Степень прогрессирования легочной гипертензии, безусловно, прямо пропорциональна величине дефекта и возрасту больных. Однако в силу индивидуальных особенностей организма и неизвестных пока причин при одинаковой величине дефекта у одних больных легочная гипертензия может быстро прогрессировать с развитием склеротической стадии в течение одного-двух лет, что вероятно связано с задержкой фетального формирования сосудов легких и частичным сохранением внутриутробного типа строения, а у других пациентов, несмотря на наличие у них большого артериовенозного сброса крови, в течение двух десятилетий могут сохраняться невысокие величины давления в легочной артерии и общелегочного сопротивления.
Важным фактором оценки тяжести состояния больного служит степень выраженности недостаточности кровообращения. Сердечная недостаточность при врожденном пороке сердца чаще бывает двусторонней, реже — односторонней (в частности, при изолированном стенозе легочной артерии, транспозиции магистральных сосудов и др. отмечается преимущественно правожелудочковая недостаточность, при стенозе устья аорты или коарктации аорты — левожелудочковая декомпенсация). Сердечная декомпенсация и цианоз наиболее часто встречаются и тяжело протекают в периоде новорожденности. Выживаемость пациентов с врожденным пороком сердца и наличием сердечной недостаточности или цианоза в возрасте до одного года составляет 30—50%, а при их сочетании — лишь 20%.
Нередко врожденный порок сердца осложняются различными нарушениями ритма сердца и проводимости в виде приступов пароксизмальной тахикардии и мерцательной аритмии, блокады ножек пучка Гиса или атриовенгрикулярнои блокады, которые в основном наблюдаются в терминальной фазе заболевания. Для пороков с обогащением малого круга кровообращения характерны рецидивирующие пневмонии и бронхиты уже в раннем детском возрасте с последующим развитием хронических неспецифических заболеваний легких (хронические неспецифические заболевания легких) У пациентов с врожденным пороком сердца, при которых имеют место большой перепад давления между полостями сердца, а также сосудов и высокая скорость кровотока через дефект (тетрада Фалло, дефект межжелудочковой перегородки, открытый артериальный проток, стеноз устья аорты и др ) отмечается предрасположенность к осложнению врожденных пороков сердца инфекционным (септическим) эндокардитом (частота встречаемости 3,3—23 1000) Так, из 226 детей, перенесших инфекционный эндокардит, у 24% обнаруживалась тетрада Фалло, у 16% — дефект межжелудочковой перегородки, у 10-12% — клапанный стеноз аорты, у 7% — открытый артериальный проток, у 26% — другие врожденные пороки сердца.
РЦРЗ (Республиканский центр развития здравоохранения МЗ РК)
Версия: Клинические протоколы МЗ РК — 2013
Общая информация
Пневмония представляет собой воспалительное заболевание легких, диагностируемое по синдрому дыхательных расстройств и физикальным данным при наличии инфильтративных изменений на рентгенограмме.
Классификация
Диагностика
Дифференциальный диагноз
| Диагноз или причина заболевания | В пользу диагноза |
| Пневмония | |
| Бронхиолит | |
| Туберкулез | |
| Инородное тело | |
| Выпот/эмпиема плевры | |
| Пневмоторакс | |
| Пневмоцистная пневмония | |
| Сердечная недостаточность, пороки сердца | |
| Врожденный порок сердца | |
| Тяжелая анемия | Получить консультацию по медтуризму Получить консультацию по медтуризму — улучшение самочувствия и аппетита. — Антибиотикотерапия (по стандарту ИВБДВ): препараты выбора – ампициллин (50 мг/кг) в/м или в/в каждые 6 часов и гентамицин (7,5 мг/кг) в/м или в/в 1 раз в день в течение 5 дней. Если состояние не улучшается в течение 48 часов, переходите на лечение гентамицином (7,5 мг/кг) в/м или в/в 1 раз в день и клоксациллином (50 мг/кг) в/м или в/в через каждые 6 часов. При неэффективности лечения антибиотиками первой линии должен назначаться цефтриаксон (80 мг/кг в сутки) в/м или в/в 1 раз в день в течение 5 дней в качестве второй линии. — Не использовать противокашлевые препараты (средства, подавляющие кашель) и отхаркивающие средства детям до 5 лет; Антибиотиками первого выбора для детей старше 5 лет являются амоксициллин и макролиды, альтернативными — амоксициллин/клавуланат, цефуроксим аксетил. У детей со склонностью к аллергическим реакциям предпочтительно назначать современные макролиды. Препаратами выбора при атипичных формах являются современные макролиды (азитромицин, эритромицин, ровамицин). При анаэробной инфекции эффективны ингибиторозащищенные пенициллины, линкомицин, клиндамицин, метронидазол, карбапенемы (меропенем разрешен к применению у детей в возрасте от 3 мес), при пневмоцистной инфекции – котримоксазол в высоких дозах (8 мг/кг триметоприма и 40 мг/кг сульфаметоксазола в/в каждые 8 часов или орально 3 раза в день) в течение 3 недель. Пневмонии детей с иммунодефицитом. Для эмпирической терапии у лиц с бактериальной природой пневмонии используют цефалоспорины III-IV поколений или ванкомицин в сочетании с аминогликозидами (нетилмицин, амикацин). При пневмоцистной этиологии пневмонии применяется котримоксазол в высоких дозах, при грибковой инфекции — противогрибковые препараты (флуконазол, амфотерицин В), герпетической инфекции — ацикловир, при цитомегаловирусной инфекции — ганцикловир. Длительность терапии составляет не менее 3 нед, при протозойной и грибковой пневмониях — 4-6 нед и более. — Дети, перенесшие пневмонию, находятся на диспансерном наблюдении в течение 1 года (осмотры проводят через 1, 3, 6 и 12 месяцев). (No Ratings Yet) Загрузка… Adblock |
Источник