Ожог мозга у человека что такое
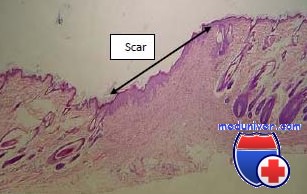
Нервная система при ожоге. Изменения гипофиза при ожоговой болезни
При обугливании сосочкового слоя собственно кожи издают относительно узкую неправильных очертаний полосу черного цвета, имеющую гомогенный или глыбчатый вид. Обугливание сетчатого слоя под микроскопом напоминает вспученную ткань, представляющую собой крупнопетлистую сеть причудливых очертаний, верхние отделы которой черного цвета, а нижние— коричневого. Только самые глубокие участки сетчатого слоя имеют вид спрессованной гомогенной ткани желтоватого цвета с базофильным оттенком.
Аналогичного вида и подкожная жировая клетчатка, в которой контуры жировых клеток и сосудов почти не определяются.
Подлежащая мышечная ткань имеет желтовато-розовый цвет. Структура ткани обычно сохранена: определяются мышечные пучки, отельные мышечные волокна, перимизий. Эндомизий не выявляется, так как набухшие мышечные волокна плотно при лежат друг к другу. Поперечная исчерченность местами сохранена, местами волокна имеют гомогенный вид. В некоторых волок пах заметны ядра. Сосуды спавшиеся.
В случаях смерти в пожаре реактивные изменения при глубоком обугливании бывают выражены слабо в связи с тем, что такое обугливание происходит уже после наступления смерти Поэтому практическое значение имеет исследование не столько обугленных тканей, сколько пограничных с ними участков.
В коже здесь довольно часто находят дистрофические и некробиотические изменения клеток эпидермиса, образование микропузырей, на рушение реологических свойств крови, сосудистую реакцию, кровоизлияния, тромбы.
Изменения в нервной системе и во внутренних органах различны в зависимости от стадии ожоговой болезни. Здесь приводятся только ранние изменения, которые возникают в период ожогового шока (в пределах четырех суток после ожогов).

В мягких мозговых оболочках отмечают полнокровие артерий и вен, разрыхление и отек волокнистого каркаса субарахноидального пространства. В мозговой ткани вначале преобладает неравномерное кровенаполнение вследствие спазма многих капилляров и артериол. Однако оно быстро сменяется сосудистыми изменениями типа дистонии и полнокровием мелких сосудов. В них наблюдают агрегацию эритроцитов и стазы. Периваскулярная ткань разрыхлена.
Встречаются точечные кровоизлияния. Невроциты увеличены в размерах, приобретают округлую форму, отростки утолщены и могут становиться видимыми при окраске гематоксилин-эозином. В цитоплазме появляются вакуоли и отмечается центральное пли тотальное растворение базофильного вещества. В нервных клетках пшоталамическпх ядер к 18—20-му ч содержится умеренное количество нейросекреторных гранул, располагающихся, как обычно, перинуклеарно.
Одновременно в их цитоплазме обнаруживают мелкие вакуоли. В отдельных клетках встречают и крупные вакуоли; они оттесняют ядро к периферии клетки, придавая ему полулунную форму. В таких клетках нейросекрет отсутствует. К 24—30-му часу число вакуольно-перерожденных клеток увеличивается.
В гипофизе в период ожогового шока изменения имеют фазный характер. В передней доле через 6 ч отмечают расширение синусоидов при умеренном их кровенаполнении и некоторое набухание стромы. Главные клетки остаются преобладающими над эозинофильными и базофильными; при этом количество эозинофилов и базофилов обычное. По истечении 10—12 ч полнокровие становится резким, распространяется и на заднюю долю, местами имеет характер паретического; могут наблюдаться стазы. В клеточном составе происходят сдвиги.
Увеличивается количество базофильных клеток. При специальных окрасках в их цитоплазме обнаруживают большое количество альдегидфуксинофильных гранул и зерен гликопротеидов. К 24—30-му часу, помимо значительного полнокровия синусоидов и увеличения числа базофильных клеток, отмечают резкое набухание тел и ядер клеток, дегрануляцию. Некоторое число базофильных и эозинофильных клеток находится в состоянии дистрофии — их цитоплазма становится мутной, содержит вакуоли, а альдегидфуксинофильные гранулы и зерна гликопротеида из нее исчезают. В последующем количество базофилов резко уменьшается, дистрофические явления захватывают все большее число клеток. Отмечают выраженный гиперхроматоз ядер эндотелия.
В задней доле гипофиза через 6 ч обнаруживают незначительное содержание нейросекрета в виде гналиноподобных глыбок различной величины. Позднее — к 12—18-му часу его содержание становится высоким, он скапливается около сосудов (поступление секрета в кровь задерживается). Ядра питуицитов оказываются насыщенными ДНК.
– Также рекомендуем “Надпочечники при ожоговой болезни. Паренхиматозные органы при ожогах”
Оглавление темы “Термические ожоги. Общее переохлаждение”:
1. Планктон. Диатомный планктон при утоплении
2. Изменения органов при утоплении. Головной мозг, сердце, печень при утоплении
3. Ожоги. Местные проявления ожогов
4. Изменения кожи при ожоге. Эпидермис при ожоге
5. Коагуляционный некроз при ожоге. Морфология четвертой степени ожога
6. Нервная система при ожоге. Изменения гипофиза при ожоговой болезни
7. Надпочечники при ожоговой болезни. Паренхиматозные органы при ожогах
8. Общее переохлаждение. Признаки смерти от общего переохлаждения
9. Отморожение кожи. Признаки отморожения кожи
10. Органы при общем переохлаждении. Поражение электрическим током
Источник
© С.Е. Хрулев, А.Н.Белова, И.Д.Булюбаш,
С.В.Евстигнеев, А.Л. Борисевич, М.В.Растеряева, 2002 г.
УДК 616.831—001.17
Поступила 29.11.2001 г.
С.Е.Хрулев, А.Н.Белова, И.Д.Булюбаш, С.В.Евстигнеев, А.Л.Борисевич, М.В.Растеряева
Научно-исследовательский институт травматологии и ортопедии, Нижний Новгород
Профилактика и лечение поражений головного мозга при ожоговой болезни
К числу наименее изученных вопросов комбустиологии относится проблема поражения нервной системы при термической травме. Ожоговая болезнь — яркий пример полиорганной недостаточности. Одним из проявлений этой недостаточности является поражение головного мозга, которое наиболее часто манифестирует острой ожоговой энцефалопатией [1]. Помимо энцефалопатии церебральная патология при ожоговой болезни может проявляться в форме делирия и мозгового инсульта. Все эти патологические состояния до настоящего времени изучены недостаточно полно. Существующие публикации по лечению неврологических осложнений термической травмы в основном касаются коррекции эмоционально-волевых расстройств и нарушений когнитивных функций в поздних периодах ожоговой болезни [2, 3]. Таким образом, адресная специфическая профилактика и терапия различных вариантов поражения головного мозга, проводимая с учетом риска их развития при ожоговой травме, является весьма актуальной проблемой.
Цель исследования — выявление факторов риска развития энцефалопатии, делирия и острого нарушения мозгового кровообращения у обожженных и разработка мер профилактики и лечения данных состояний.
Материалы и методы.
Исследование проводилось в клинике Российского ожогового центра (РОЦ) на базе Нижегородского НИИ травматологии и ортопедии. Работа осуществлялась в два этапа: 1) выявление факторов риска развития энцефалопатии, делирия и острого нарушения мозгового кровообращения у обожженных; 2) разработка схем профилактики и лечения данных состояний и оценка их эффективности.
На первом этапе обследовано 160 ожоговых больных, прошедших лечение в РОЦ в 1999—2000 гг., в возрасте от 16 до 75 лет, с площадью поражения от 5 до 75% поверхности тела. Среди них у 68 человек выявлена клиника энцефалопатии (средний возраст 51±8 лет, средняя площадь поражения 38±15%), у 3 человек отмечено развитие инсульта (средний возраст 59±8 лет, средняя площадь поражения 30±17% поверхности тела); у 10 больных развился делирий (средний возраст 43±14 лет, средняя площадь поражения 46±16% поверхности тела). Кроме того, взяты из архива и обработаны данные 18 историй болезни пациентов, перенесших в период термической травмы мозговой инсульт (с 1985 по 1998 гг.).
Для определения факторов, игравших решающую роль в развитии той или иной формы церебральной патологии, был проведен дисперсионный анализ 16 параметров, отражавших пол, возраст, характер и тяжесть ожоговой травмы, данные анамнеза жизни, лабораторные показатели. Определение критических значений выявленных факторов и достоверность их влияния на развитие патологии головного мозга проводились с помощью точного критерия Фишера.
На втором этапе работы обследовано 148 больных, проходивших лечение в РОЦ в 2000—2001 гг., из них профилактические и специализированные лечебные мероприятия проведены 75 больным, имевшим высокий риск развития различной церебральной патологии (основная группа). В данной группе 60 пострадавших имели высокий риск развития энцефалопатии разной степени тяжести (средний возраст 52±7 лет, площадь ожога 42±4% поверхности тела), 10 человек (средний возраст 57±7 лет, площадь ожога 25±13% поверхности тела) — мозгового инсульта и 8 человек (средний возраст 49±17 лет, площадь ожога 37±13% поверхности тела) — делирия.
Оценка эффективности мер профилактики и лечения проводилась путем сравнения результатов, достигнутых в основной группе, и у 80 больных, сопоставимых с пациентами основной группы по возрасту, тяжести ожоговой травмы и по степени риска развития церебральной патологии, но не получавших соответствующих профилактических и лечебных воздействий (группа сравнения).
Результаты и обсуждение.
Выявленным в результате исследования факторам риска развития энцефалопатии, делирия и инсульта у обожженных методом экспертной оценки был придан индекс значимости, выраженный в баллах (1, 2 и 3 балла). Чем больше индекс значимости, тем важнее фактор в прогностическом отношении (см. таблицу).
| Факторы риска развития энцефалопатии, делирия и инсульта у обожженных |
Для определения вероятности развития ожоговой энцефалопатии необходимо при поступлении больного в отделение оценить наличие и выраженность у него ожоговой болезни, величину индекса тяжести поражения*, наличие в анамнезе черепно-мозговых травм, сопутствующей гипертонической болезни, хронического алкоголизма, а также учесть возраст пациента. Далее производится суммирование баллов. Если тот или иной фактор отсутствует, проставляется балл «0». Оценка выявленных факторов риска в баллах при поступлении может варьировать от
0 до 10. Результаты проведенных исследований позволили установить следующую закономерность: при сумме баллов от 0 до 2 риск развития энцефалопатии достаточно низкий (11%), при сумме от 3 до 5 он повышается до 66%; при сумме, равной 6 баллам и выше, вероятность развития энцефалопатии равна 98% (p4.
Для определения вероятности развития делирия выявляют данные анамнеза о злоупотреблениях алкоголем в виде эпизодов запойного пьянства, вычисляют индекс тяжести поражения и уровень аланинаминотрансферазы крови. Процедура суммирования баллов аналогична вышеописанной. Оценка выявленных факторов риска в баллах при поступлении может варьировать от
0 до 3. Больной, набравший в сумме 3 балла, имеет 100%-ный риск развития делирия; при сумме
2 балла вероятность возникновения делирия — 32%; при оценке в 0—1 балл вероятность присоединения делирия крайне низкая (p5.
Для определения вероятности развития инсульта необходимо при поступлении больного в отделение оценить величину индекса тяжести поражения, наличие в анамнезе данных о перенесенных нарушениях мозгового кровообращения, алкоголизме, сопутствующих гипертонической болезни и ишемической болезни сердца, а также учесть возраст пациента. Оценка факторов риска инсульта в баллах при поступлении может варьировать от 0 до 10 баллов. При оценке в 3—4 балла вероятность развития инсульта равна 33,3%; при 5—6 баллах — 62,5%, при сумме 7—8 баллов она увеличивается до 80% и при 9—10 баллах достигает 100% (p6.
Итогом первого этапа работы стало выделение групп риска по развитию у больных с ожогами различных клинических вариантов поражения головного мозга.
На втором этапе исследования разработаны и апробированы дифференцированные схемы профилактики и лечения церебральных осложнений у обожженных.
Больным с риском развития церебральной патологии, превышающим 70%, профилактически (начиная со стадии шока) назначались препараты, улучшающие метаболизм головного мозга, микроциркуляцию и церебральное кровообращение, направленные на борьбу с отеком головного мозга при наличии внутричерепной гипертензии. Из всего многообразия препаратов, улучшающих церебральный метаболизм, нами выбраны ноотропил, церебролизин и актовегин как наиболее эффективные и имеющие минимальное количество осложнений 7. Церебролизин обладает нейромодулирующим, нейропротекторным и нейротрофическим действием. Ноотропил повышает энергетический обмен клеток головного мозга, улучшает интегративную деятельность мозга, способствует консолидации памяти. Актовегин, помимо положительного воздействия на метаболизм и кровообращение головного мозга, оказывает выраженное антиоксидантное действие и способствует репаративным процессам, что представляется крайне важным при ожоговой травме.
Из препаратов, улучшающих кровообращение головного мозга, был выбран инстенон как эффективный препарат, обладающий минимальной кардиотоксичностью (в отличие, например, от кавинтона). Инстенон является единственным кобинированным ноотропным препаратом, сочетающим к себе истинно ноотропный, сосудистый и нейростимулирующий компоненты, что дает возможность комплексного воздействия на различные звенья патогенеза ишемии и гипоксии головного мозга 7. Ограничением к назначению инстенона у обожженных служила клиника выраженного повышения внутричерепного давления, препарат не использовался также при эпилептическом синдроме, подозрении на внутримозговое кровоизлияние.
Кроме того, при высоком риске инсульта для улучшения микроциркуляции головного мозга нами использовался тиклид, который тормозит агрегацию и адгезию тромбоцитов, а также снижает оседание тромбоцитов на атеросклеротической бляшке у пациентов с цереброваскулярными заболеваниями. Из препаратов, уменьшающих отек головного мозга, отдано предпочтение диакарбу (фонуриту), который помимо мочегонного действия, обладает противосудорожной активностью.
Для профилактики и лечения делирия использовался нейролептик тиапридал, который наряду с антипсихотическим и анксиолитическим действием способствует ясности мышления и имеет выраженный анальгезирующий эффект.
При ожоговой травме в течение многих лет успешно используется магния сульфат в качестве дегидратационного средства, который обладает еще и дезинтоксикационным, противосудорожным и седативным эффектом. Подбор наиболее эффективных неврологических препаратов с учетом не только их основного действия, но и сопутствующих эффектов позволил избежать полипрагмазии, что крайне важно при полиорганной недостаточности.
С целью профилактики поражений головного мозга использовались следующие схемы приема препаратов.
Для профилактики энцефалопатии ноотропил применяли в дозе 5 мл внутривенно струйно 1 раз в сутки в течение 10 дней; актовегин — в дозе 2 мл (80 мг) внутривенно 1 раз в сутки в течение 10 дней.
Профилактика развития делирия заключалась в назначении седативной, психотропной терапии, витаминов, препаратов, улучшающих церебральный метаболизм и кровообращение. Использовалась следующая схема: реланиум — 2 мл 2 раза в сутки в течение 2—3 дней, тиапридал — внутримышечно 2 мл 2 раза в сутки; магния сульфат 25% — 10 мл 1 раз в сутки в течение 5—7 дней; ноотропил, актовегин в вышеуказанных дозировках; витамины В1 6% — 3 мл 2 раза в сутки, В6 5% — по 3 мл 2 раза в сутки в течение 7—10 дней, аскорбиновая кислота 5% — 0,3—1 мл 3 раза в сутки в течение 5 дней. Лечение осуществлялось на фоне усиления дезинтоксикационной терапии, проведения плазмафереза с частотой 2—3 раза в неделю.
Мероприятия по профилактике острых нарушений мозгового кровообращения зависели от наличия или отсутствия признаков внутричерепной гипертензии. Если клинические данные о повышении внутричерепного давления отсутствовали, то назначались ноотропил — 5 мл внутривенно струйно 2 раза в сутки в течение 15 дней; актовегин — 5 мл (200 мг) внутривенно 2 раза в сутки в течение 10 дней, либо актовегин 5 мл (200 мг) внутривенно 1 раз в сутки в течение 10 дней и инстенон — 2 мл на 0,9% физрастворе внутривенно медленно (в течение 2—3 ч) 1 раз в сутки в течение 7 дней; тиклид — 250 мг 2 раза в сутки в течение 15 дней. Затем переходили на пероральный прием препаратов в течение 1—2 мес. Если у больного имелись клинические проявления внутричерепной гипертензии (головная боль, нарушение сознания, изменения психики, менингеальные симптомы), то в первую очередь добивались снижения внутричерепного давления. Для этого головному концу кровати придавали возвышенное положение на 10—15%, ограничивали объем вводимой жидкости (разница между объемом потребляемой и выделяемой жидкости не должна была превышать 1,5 л в сутки); назначали диакарб — 250 мг утром через день в течение 2—3 нед под контролем содержания калия в сыворотке крови (не ниже 3,3 ммоль/л). Применяли препараты: тиклид — 250 мг 2 раза в сутки в течение 15 дней, церебролизин — 5 мл внутривенно 2 раза в сутки в течение 15 дней или ноотропил — 5 мл внутривенно струйно 2 раза в сутки в течение 15 дней, актовегин — 5 мл внутривенно капельно 2 раза в сутки в течение 10 дней, затем переходили на пероральный прием этих же препаратов в течение 1—2 мес. При необходимости курсы ноотропов и сосудистых препаратов повторяли.
Несмотря на проводимые профилактические мероприятия, полностью предотвратить развитие церебральных нарушений при ожоговой болезни очень сложно. Нами разработаны комплексы лечебных воздействий при развитии различных форм поражений головного мозга. Лечение церебральной патологии проводилось на фоне стандартной инфузионно-трансфузионной терапии, применяемой при ожоговой болезни.
При развитии проявлений энцефалопатии легкой степени у обожженных назначались ноотропил в дозе 5 мл внутривенно струйно 2 раза в сутки в течение 10 дней; актовегин — 4 мл
(160 мг) внутривенно один раз в сутки в течение 10 дней. У больных с тяжелой энцефалопатией лечение различалось в зависимости от наличия внутричерепной гипертензии. При отсутствии признаков повышения внутричерепного давления: ноотропил — 10 мл внутривенно струйно 2 раза в сутки в течение 15 дней; актовегин — 6 мл (240 мг) внутривенно 2 раза в сутки в течение 15 дней либо актовегин — 6 мл (240 мг) внутривенно 1 раз в сутки на 0,9% физрастворе в течение 15 дней в комбинации с инстеноном — 2 мл внутривенно капельно медленно (в течение 2—3 ч) 1 раз в сутки в течение 7 дней; тиклид — 250 мг 2 раза в сутки в течение 25 дней. Затем переходили на пероральный прием препаратов в течение 1 мес. При наличии явлений внутричерепной гипертензии больным устанавливали возвышенное положение головного конца кровати на 10—15°, ограничивали объем вводимой жидкости; назначали диакарб — 250 мг утром через день в течение месяца; тиклид — 250 мг 2 раза в сутки на протяжении 25 дней; церебролизин — 10 мл внутривенно 2 раза в сутки в течение 15 дней. Затем переходили на пероральный прием этих препаратов в течение 1 мес. При необходимости курсы ноотропов и сосудистых препаратов повторяли.
У больных с делирием, развившимся на фоне ожоговой травмы, применялась следующая терапия: реланиум — 2 мл 2—3 раза в сутки в течение 2—3 дней, при продолжающихся приступах психомоторного возбуждения — ГОМК — 6 мл в сутки; тиапридал — внутримышечно 2 мл 3—4 раза в сутки; магния сульфат 25% — 10 мл 2 раза в сутки в течение 5—7 дней, витамины: В1 6% — 3 мл 2 раза в сутки, В6 5% — 3 мл 2 раза в сутки в течение 7—10 дней, 5% аскорбиновая кислота — 1 мл 3 раза в день в течение 5 дней; сосудистые препараты, ноотропы (по предложенным выше схемам); усиление дезинтоксикационных мероприятий (проведение ежедневного плазмафереза).
Для лечения инсульта схемы воздействий различаются в зависимости от наличия симптомов повышения внутричерепного давления. При отсутствии клиники внутричерепной гипертензии терапия заключалась в назначении ноотропила — 10 мл внутривенно струйно 2 раза в сутки в течение 15 дней; актовегина — 8—10 мл (360—400 мг) внутривенно 2 раза в сутки в течение 15 дней либо актовегина — 8—10 мл (360—400 мг) внутривенно один раз в сутки в течение 15 дней и инстенона — 2 мл внутривенно капельно медленно (в течение 2—3 ч) один раз в сутки на протяжении 7 дней; тиклида — 250 мг 2 раза в сутки в течение 25 дней. Затем продолжали пероральный прием препаратов в течение 1—2 мес. У больных с явлением внутричерепной гипертензии устанавливали возвышенное положение головного конца кровати на 10—15°; производилось ограничение объема вводимой жидкости, назначались диакарб — 250 мг утром через день в течение месяца, тиклид — 250 мг 2 раза в сутки на протяжении 25 дней, церебролизин — 10 мл внутривенно 2 раза в сутки в течение 15 дней; актовегин — 8—10 мл (360—400 мг) внутривенно капельно 2 раза в сутки в течение 15 дней. Затем переходили на пероральный прием этих же препаратов в течение 1—2 мес. При необходимости курсы ноотропов и сосудистых препаратов повторяли.
По результатам исследований была определена эффективность проводимых профилактических и лечебных воздействий. Частота развития энцефалопатии в основной группе составила 35,1%, тогда как в группе сравнения — 42,5% (p
При оценке факторов риска развитие инсульта с вероятностью более 80% можно было ожидать у 10 больных основной группы и у 3 больных группы сравнения. При этом в основной группе инсульт реально развился лишь у 2 больных, т.е. благодаря проведенным профилактическим мероприятиям удалось предотвратить не менее 8 инсультов. Несмотря на развитие инсультов, оба больных выжили, что свидетельствует об эффективности проводимой терапии. В то же время в группе сравнения, получавшей традиционное лечение, инсульт развился в 3 случаях из 3 прогнозируемых, причем все они закончились летальным исходом. Надо отметить, что в одном из этих случаев инсульт явился непосредственной причиной смертельного исхода, в остальных же, несомненно, способствовал ему.
В основной группе делирий развился в 4 из 8 прогнозируемых случаев (у 4 больных его развитие удалось предотвратить), в то время как в группе сравнения делирий развился у всех 10 больных с высоким риском его развития. В основной группе из 4 больных с развившимся делирием умерло 2 пациента, в группе сравнения смертельным исходом закончились 7 случаев из 10.
Заключение.
Результаты проведенных исследований убедительно свидетельствуют, что профилактические мероприятия, основанные на выделении среди обожженных групп риска по развитию энцефалопатии, делирия и инсульта и своевременной адекватной терапии этих состояний, достоверно снижают частоту появления церебральной патологии и случаев летального исхода при ней, а также способствуют сокращению длительности пребывания больного в стационаре в острый период.
Литература
Лейдерман И.Н. Синдром полиорганной недостаточности, метаболические основы. Вестник интенсивной терапии 1999; 2: 5—10.
Волошин П.В. Патология нервной системы при ожоговой болезни. Киев: Здоровье; 1982.
Гельфанд В.Б., Николаев Г.В. Нервно-психические расстройства при термических повреждениях. Сов мед 1985; 2: 74—78.
Хрулев С.Е., Белова А.Н., Евстигнеев С.В. и др. Реабилитация обожженных с позиций невролога. В кн.: Материалы I Межрегиональной конференции «Проблемы восстановительной медицины». Воронеж; 2001.
Хрулев С.Е., Белова А.Н., Стручков А.А. и др. Ожоговая энцефалопатия: степени тяжести и факторы риска. В кн.: Материалы юбил. научн. конф., посвященной 140-летию кафедры душевных и нервных болезней военно-медицинской академии. СПб; 2000.
Хрулев С.Е., Белова А.Н., Стручков А.А. и др. Делирий как проявление ожоговой энцефалопатии. В кн.: Материалы VIII Всерос. съезда неврологов. Казань; 2001.
Бурцев С.В. Нейрометаболическая фармакотерапия. М; 2000.
Источник
