Лечение лучевых ожогов мочевого пузыря

Лучевой цистит – это реакция тканей мочевого пузыря на ионизирующее облучение, проводимое в рамках лечения злокачественных опухолей малого таза. Симптомы зависят от полученной лучевой нагрузки, варьируются от незначительного дискомфорта при мочеиспускании, частых позывов и микрогематурии до выраженных болей, появления рецидивирующего кровотечения, угрожающего жизни. Диагноз подтверждают с помощью общего анализа мочи, цистоскопии. Лечение пострадиационного цистита определяется степенью выраженности поражения, может быть консервативным или оперативным с выполнением цистэктомии, решением вопроса с отведением мочи.
Общие сведения
Лучевой цистит регистрируют у 5-21% пациентов как осложнение лучевой терапии. Наиболее часто симптомы появляются после лечения рака мочевого пузыря (18%), простаты (14%), шейки матки (5%). Патология развивается в среднем через 32 недели после лечения, у мужчин чаще, чем у женщин (2,8:1). Конформная лучевая терапия, брахитерапия сопряжены с меньшей вероятностью возникновения пострадиационного цистита по сравнению с обычной. Но даже при таком лечении случайное облучение близлежащих тканей неизбежно из-за проникновения новообразования в окружающие органы или из-за близости рака к соседним структурам таза.
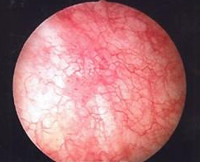
Лучевой цистит
Причины
Во время лучевой терапии происходит передача энергии ионизирующего излучения молекулам опухолевых клеток и тканям соседних органов, в частности – мочевому пузырю, прямой кишке. В результате альтерации нарушается трофика, кровоснабжение, позднее развиваются фиброзно-склерозирующие изменения. Пострадиационный цистит вызывает прохождение лучевой терапии по поводу опухолей:
- предстательной железы;
- влагалища, матки, ее шейки, яичников;
- мочевого пузыря;
- толстой, прямой кишки.
Определенное значение имеют локализация новообразования, стадия болезни, ежедневная и суммарная доза облучения (количество сеансов), тип лучевой терапии. К способствующим циститу факторам относятся:
- общее снижение иммунной реактивности организма на фоне злокачественного новообразования;
- выполненное оперативное вмешательство, например, трансуретральная резекция (ТУР) простаты или стенки пузыря с опухолью;
- одновременное прохождение химиотерапии;
- урологические заболевания: сопутствующий воспалительный процесс, цистолитиаз, дивертикулы;
- патологии, предрасполагающие к плохому заживлению, локальной ишемии: СПИД, сахарный диабет, болезни сосудов;
- ожирение (ИМТ >30 кг/м2);
- проведение гормонального лечения по поводу рака простаты;
- хроническая никотиновая интоксикация (≥1 пачки в день).
Патогенез
Радиация взаимодействует с внутриклеточной жидкостью, в результате высвобождаются свободные радикалы, нарушающие синтез ДНК, что приводит к гибели клеток. На фоне терапии повреждаются мембраны как раковых, так и здоровых клеток, изменения затрагивают сосуды. Субэндотелиальная пролиферация, отек постепенно истощают кровоснабжение облученной зоны. Неоваскуляризация, неадекватная регенерация провоцируют формирование хрупких поверхностных сосудов, ответственных за макрогематурию при геморрагическом цистите.
Отложение коллагена запускает процессы рубцевания, способствует дальнейшей облитерации кровеносных сосудов, вследствие чего развивается гипоксия, некроз. В мочевом пузыре на фоне ишемии слизистой оболочки повреждается уротелий, что вызывает подслизистый фиброз, поскольку субэпителиальные ткани подвергаются едкому воздействию мочи. Образование язв, поражение нервов, пострадиационный фиброз обеспечивают появление развернутой клинической симптоматики.
Классификация
Лучевой цистит может быть ранним, возникающим в течение 4 недель или 6-12 месяцев после терапии, и поздним, с появлением симптомов спустя год или позже. Выделяют острое и хроническое течение пострадиационного воспаления. Специалисты в сфере онкоурологии используют в работе специальную шкалу для оценки степени выраженности изменений мочевого пузыря, подвергшегося лучевому воздействию:
- 1 степень подразумевает незначительную эпителиальную атрофию и расширение сосудов, обнаружение единичных эритроцитов в моче. Клинические проявления чаще отсутствуют.
- 2 степень характеризуется обнаружением множественных телеангиэктазий, эпизодами макрогематурии. Мочеиспускание учащено, появляются жалобы на недержание урины.
- 3 степень представлена видоизменением сосудов по всей поверхности, формированием микроциста (уменьшением емкости органа), стойким недержанием мочи, изнурительными позывами на мочевыделение до 40 эпизодов в сутки, включая ноктурию, рецидивирующей макрогематурией.
- 4 степень при цистоскопии обнаруживаются участки некротизации, признаки тотального геморрагического цистита с участками петехий, емкость пузыря при тугом наполнении менее 100 мл, отмечается полная утрата контроля над мочевыделением, требующая вспомогательных мер (катетеризации или цистэктомии). В моче постоянно присутствует кровь, белок, слущенный эпителий.
- 5 степень наиболее неблагоприятна в прогностическом плане, гематурия приводит к развитию угрожающей жизни анемии, формированию свищей. Определяется максимально выраженный болевой синдром, высокий риск летального исхода.
Симптомы лучевого цистита
Сразу или через несколько недель после одномоментного получения значительной дозы радиации развивается острый воспалительный процесс. Как правило, ранний цистит является самоограниченным, симптомы аналогичны острому инфекционному воспалению, включают рези при учащенном мочеиспускании и после, боли внизу живота, ургентные позывы на мочевыделение. Может присутствовать кровь в моче, но более типична микрогематурия. Отмечается хороший ответ на терапию.
Лучевой цистит, возникший спустя несколько месяцев либо лет после лечения, может проявляться постоянной дизурией, сильной болью, позывами к мочеиспусканию через каждые 10-15 минут из-за формирования микроциста, выделением урины с кровью, стойкой инконтиненцией. Макрогематурия приобретает рецидивирующий характер, обнаруживается значительная кровопотеря. Повышение температуры свидетельствует о вторичном бактериальном инфицировании.
Осложнения
Лучевой цистит осложняется присоединением инфекции с развитием бактериального воспалительного процесса в почках (пиелонефрит в 20%), прогрессирующим уменьшением емкости или рубцовым сморщиванием органа и неоплазией (менее 2%), образованием свища (2%), контрактуры шейки (3-5%). При выраженном пострадиационном воспалении возникает некупируемый хронический болевой синдром, значительно ухудшающий качество жизни.
Кровотечению из видоизмененных сосудов (геморрагический цистит в 3-5%) нередко сопутствует анемия, иногда частота и выраженность кровотечения настолько значительна, что требуется проведение цистэктомии, поскольку неоднократные коагуляции лишь усугубляют фиброзно-склеротический процесс. Гематурия может сопровождаться образованием сгустков, которые приводят к острой задержке мочеиспускания за счет гемотампонады уретры.
Диагностика
Прохождение лечения с использованием ионизирующего облучения с отсроченным появлением типичных жалоб – основной критерий, на основании которого врач-уролог выставляет предварительный диагноз лучевого цистита. Учитывая то, что данные симптомы могут свидетельствовать о ряде других патологических процессов, показано прохождение углубленного клинико-урологического обследования, которое включает:
- Лабораторные анализы. В ОАМ обнаруживают микро- или макрогематурию, белок, эпителий, иногда бактерии, лейкоциты. Бакпосев производят для исключения инфекции мочевыводящих путей. Цитология мочи обоснована при подозрении на рак мочевого пузыря. В результатах анализа крови обращают внимание на гемоглобин, гематокрит, уровень тромбоцитов. Коагулограмма позволяет исключить нарушения в работе свертывающей системы.
- Инструментальную диагностику. Основным исследованием является цистоскопия, которая позволяет исключить другие причины жалоб, например, камень или мочепузырную опухоль. Типичная картина – множественные телеангиэктазии на фоне отечной слизистой, на продвинутой стадии – множественные эрозии. Прочие методы визуализации (МРТ, КТ, экскреторную урографию) назначают для исключения свищей, других причин гематурии.
- Биопсию стенки пузыря. Морфологическое исследование проводят после получения неоднозначных результатов УЗИ, цистоскопии и КТ или МРТ при высокой вероятности опухолевого процесса. Перед выполнением биопсии учитывают потенциальный риск кровотечения из поверхностных сосудов в результате травматизации.
Дифференциацию осуществляют между уроцистолитиазом, распространением опухоли из малого таза в пузырь, прогрессированием рака, сопровождающегося кровотечением, болевым синдромом. КТ и МРТ становятся основными диагностическими процедурами в данной клинической ситуации.
Лечение лучевого цистита
Терапевтические мероприятия зависят от выраженности процесса, в каждом случае определяются индивидуально. Первая и вторая степени цистита после облучения требуют активной тактики только при наличии жалоб. Цистэктомия рассматривается как крайний вариант для лечения постлучевого цистита, выполняется при безуспешности консервативной терапии.
Медикаментозное лечение
Радиационно-индуцированная гематурия может быть легкой или опасной для жизни, во втором случае прибегают к реанимационным мероприятиям, переливанию компонентов крови. Перечень препаратов для лечения включает:
- антихолинергические средства;
- обезболивающие агенты;
- фибринолитики;
- лекарства, улучшающие кровообращение;
- альфа-1-адреноблокаторы.
Инстилляции в мочевой пузырь
Вливание растворов – следующий этап лечения при неэффективности пероральной терапии лучевого цистита и налаженной системы орошения. Используют следующие препараты:
- Гиалуроновая кислота. Мукополисахарид, присутствующий в соединительной и эпителиальной тканях, ингибирует образование иммунных комплексов, нейтрализует функции нейтрофилов при регуляции пролиферации фибробластов, эндотелиальных клеток. Аналогичным действием обладает хондроитин-сульфат.
- Аминокапроновая кислота. Стабилизирует процесс свертывания крови путем фибринолиза.
- Формалин. 1% раствор является тканевым фиксатором, который денатурирует поверхностный слой уротелия, обеспечивая гемостаз. Лечение сопровождается сильной болью, что требует назначения анальгетиков. Высок риск побочных эффектов.
- Соли алюминия. 1% сульфат алюминия-аммония или сульфат алюминия-калия вызывают осаждение белка на поверхности клеток и в интерстициальных пространствах, что позволяет прекратить кровоточивость.
- Плацентарный экстракт. Эффективен в эпителизации эрозий, язв.
Хирургическое лечение
Если консервативная терапия и внутрипузырные инстилляции не могут остановить кровотечение, прибегают к различным эндоскопическим или чрескожным вмешательствам. Цистоскопия с фульгурацией проблемных участков, эвакуация кровяного сгустка, выполнение электрокоагуляции являются разумными шагами в дальнейшей тактике. Виды вмешательств при лучевом цистите:
- Введение ботулинического токсина А. Препарат вводится в стенку мочевого пузыря при отсутствии эффекта от антихолинергических средств. Лечение направлено на увеличение емкости пузыря, снижение частоты мочеиспускания, купирование ургентных позывов.
- Наложение чрескожного нефростомического дренажа. Отведение мочи из ЧЛС почек способствует регенерации уротелия нижних отделов мочевого тракта. Через 3-6 месяцев восстанавливают анатомически правильный отток урины.
- Эндоскопическая склеротерапия. Введение склерозанта в кровоточащие области эффективно не в 100% случаев, но у большинства пациентов с трудноизлечимым геморрагическим циститом обеспечивает снижение выраженности симптоматики, гемостаз.
- Эмболизация сосудов. Помогает остановить кровотечение при рефрактерном пострадиационном геморрагическом цистите.
- Паллиативная цистэктомия. Органоуносящая операция показана при рецидивирующей гематурии при безуспешности всех видов лечения, формировании свища, микроцисте (объем менее 200 мл) с изнуряющими позывами на мочеиспускание, стойком болевом синдроме. Урину отводят путем создания кондуита толстой кишки или выполнения двусторонней транскутанеостомии.
Физиотерапия
Гипербарическая кислородная терапия (оксигенация) способствует нормализации ангиогенеза, мобилизации стволовых клеток, остановке кровотечения за счет активации процессов фибринолиза, разрешению ишемии. Используется как дополнительный способ лечения лучевого цистита. Проведение оксигенобаротерапии не имеет каких-либо неблагоприятных последствий.
Прогноз и профилактика
Лучевой цистит, развившийся через 4-6 недель от начала сеансов ЛТ, имеет более благоприятный прогноз. Улучшение наступает примерно через 1,5 месяца, но у 5-20% процесс переходит в стойкую форму с рецидивирующими клиническими проявлениями через несколько месяцев или даже 10-20 лет. Хронические формы менее благоприятны.
Профилактика подразумевает выбор типа лучевой терапии с максимальным воздействием на опухоль, но не на соседние ткани, выполнение инстилляций на основе гиалуроновой кислоты с превентивной целью, прием растительных диуретиков. Исследования показали уменьшение симптомов цистита при использовании добавок, содержащих клюквенный экстракт.
Источник
В статье проанализированы результаты лечения больных с поздними лучевыми повреждениями мочевого пузыря (осложненными и неосложненными циститами). Отмечается, что выбор метода лечения должен основываться на данных субъективных жалоб и объективных методов исследования. Так, при выраженном болевом синдроме и инкрустированной форме лучевого цистита наилучшие результаты отмечались на фоне внутрипузырного применения Димексида. При выраженном воспалительном процессе, сопровождающемся поверхностным нарушением слизистой мочевого пузыря, а также атрофии слизистой предпочтение следует отдать инстилляциям УРО-ГИАЛА. Рексод продемонстрировал эффективность у больных с геморрагическим синдромом, при язвенном лучевом цистите и сниженном объеме мочевого пузыря.
Таблица 1. Сравнительная характеристика результатов лечения больных первой группы до и после внутрипузырного применения Димексида
Таблица 2. Сравнительная характеристика цистоскопических признаков лучевых циститов у больных первой группы до и после внутрипузырного применения Димексида
Таблица 3. Сравнительная характеристика больных второй группы до и после внутрипузырного применения УРО-ГИАЛА
Таблица 4. Сравнительная характеристика цистоскопических признаков лучевых циститов у больных второй группы до и после внутрипузырного применения УРО-ГИАЛА
Таблица 5. Сравнительная характеристика больных третьей группы до и после внутрипузырного применения Рексода
Таблица 6. Сравнительная характеристика цистоскопических признаков лучевых циститов у больных третьей группы до и после внутрипузырного применения Рексода
Введение
В настоящее время лучевая терапия является одним из основных методов лечения злокачественных новообразований органов малого таза. При отсутствии метастазов в регионарные лимфоузлы применение лучевой терапии позволяет добиться полной или частичной регрессии опухоли (рак тела и шейки матки, рак предстательной железы, в меньшей степени рак мочевого пузыря и прямой кишки) в среднем в 70–75% случаев. При этом продолжительность жизни после окончания курса лечебных мероприятий остается относительно высокой и составляет около четырех-пяти лет [1–3].
К сожалению, у части таких больных (10–15%) формируются лучевые повреждения органов малого таза: мочевого пузыря, прямой кишки и внутритазовой клетчатки [4, 5]. Оценивая данные литературы, можно констатировать неудовлетворительные результаты диагностики и лечения лучевых повреждений органов малого таза. Это выражается в частых рецидивах цистита с исходом в сморщивание мочевого пузыря, внутритазовом лучевом фиброзе со сдавлением интрамурального и юкставезикального отделов мочеточников и развитии хронической почечной недостаточности [7–8].
Проведение лучевой терапии может осложниться развитием радиационно-индуцированного фиброза, выраженность которого прямо пропорциональна величине суммарной поглощенной дозы, режиму фракционирования и времени после проведения лучевой терапии. Микроскопическое исследование тканей с радиационно-индуцированным фиброзом показало, что его формирование сопровождается развитием каркаса в подслизистом слое стенки мочевого пузыря, в сетях которого фиксируются стенки мелких артерий и вен. Происходит лучевое повреждение и самой сосудистой стенки, особенно ее адвентиции, что приводит к потере сосудами эластичности и появлению ломкости. Клинически это обнаруживается различной степенью гематурии, вплоть до профузного кровотечения. Развитие в последующем лучевого фиброза всей стенки мочевого пузыря значительно отягощает клинические симптомы и выраженность лучевого цистита [9–11].
В диагностике лучевых циститов важное значение имеют общеклинические, рентгенологические и инструментальные методы исследования. Ведущим методом исследования мочевого пузыря остается цистоскопия, позволяющая достоверно установить локализацию и степень выраженности лучевого повреждения, то есть выявить органические изменения слизистой оболочки, наличие камней и видимых опухолевых элементов, оценить состояние устьев мочеточников.
Материал и методы
В настоящей работе проведено исследование эффективности новых методов местного лечения осложненных и неосложненных лучевых циститов. 139 больных были разделены на три группы. Первую группу составили 49 пациентов (17 с неосложненными циститами и 32 – с осложненными). Они получали традиционное местное лечение: Димексид, Колларгол, синтезоновая эмульсия и облепиховое масло. Во вторую группу вошли 52 больных (26 с неосложненными циститами и 26 – с осложненными), у которых для местного лечения использовался препарат УРО-ГИАЛ. В местной терапии третьей группы – 38 пациентов (13 с неосложненными циститами и 25 – с осложненными) – применялась супероксиддисмутаза (препарат Рексод). Кроме того, всем пациентам была назначена антибактериальная, антикоагулянтная, вазоактивная, симптоматическая и иммунная терапия.
Местное лечение больных первой группы начиналось с инстилляций 10%-ного Димексида в объеме 20 мл. Применение этого препарата патогенетически обосновано, поскольку он обладает выраженным противовоспалительным, противоотечным и обезболивающим эффектом. В связи с тем что Димексид является органическим растворителем и легко проникает в ткани, в раствор добавлялись антибиотики (гентамицин, амикацин), фибролизирующие (Лидаза) и противовоспалительные препараты (преднизолон). Инстилляции проводились ежедневно по 20 мл (от 10 до 15 процедур). У больных с микрогематурией или неинтенсивной примесью крови в моче для инстилляций мочевого пузыря дополнительно применялся 3%-ный Колларгол 20 мл на одно введение. При неэффективности монотерапии Колларголом для усиления гемостатического эффекта его чередовали с охлажденной аминокапроновой кислотой. После стихания воспалительных процессов внутрипузырно в подогретом виде один раз в сутки в течение 10–15 дней вводились синтезоновая эмульсия и облепиховое масло. Действие этих препаратов направлено на усиление репараторных процессов в стенке мочевого пузыря. Благодаря жировой основе они оказывают выраженное обволакивающее и обезболивающее действие.
Местное лечение больных второй группы подразумевало применение препарата на основе гиалуроновой кислоты УРО-ГИАЛ. УРО-ГИАЛ – вязкоэластичный протектор межклеточного вещества уротелия мочевого пузыря и уретры. УРО-ГИАЛ позволяет создать вязкоэластичную пленку на слизистой, тем самым защищая ее от агрессивного воздействия мочи и препятствуя адгезии микробов к поврежденной поверхности. Инстилляции УРО-ГИАЛА проводились через день в течение 12–15 дней, затем в режиме одно введение в неделю.
В третьей группе пациентам назначался препарат супероксиддисмутазы Рексод. Рексод прямо инактивирует свободные радикалы, блокирует реакцию перекисных радикалов с арахидоновой кислотой, ослабляет активное действие лейкотриена В4, ингибирует хемотаксис лейкоцитов, значительно уменьшает синтез коллагена фибробластами (способствует регрессии радиационно-индуцированного фиброза). Рексод вводился внутрь мочевого пузыря, при этом содержимое флакона растворяли непосредственно перед введением в 10 мл стерильного физиологического раствора. Инстилляции проводились один раз в сутки на протяжении 15–20 дней.
Результаты и обсуждение
Результаты лечения больных первой группы представлены в таблице 1. Приведенные данные свидетельствуют о значительном уменьшении частоты ночного мочеиспускания и снижении бактериурии у большинства больных как с осложненными, так и с неосложненными циститами. Несмотря на по-прежнему высокий уровень лейкоцитурии, она носила менее выраженный характер. Макрогематурия после лечения не выявлялась у пациентов с неосложненными циститами, но сохранялась у 18% пациентов с осложненными циститами.
Сравнительный анализ УЗИ-признаков лучевых циститов у больных первой группы продемонстрировал, что внутрипузырное применение Димексида позволило очистить мочевой пузырь от солевой инкрустации более чем в 50% случаев. К сожалению, основные УЗИ-признаки воспаления (взвесь в просвете мочевого пузыря и утолщение его стенок) были купированы у незначительного числа пациентов.
Динамика выраженности цистоскопических признаков лучевых циститов у больных первой группы до и после лечения продемонстрирована в таблице 2. У пациентов как с неосложненными, так и осложненными циститами сохранялись воспаление (гиперемия и отек) и телеангиоэктазии. Таким образом, внутрипузырное применение Димексида было наиболее эффективным у пациентов с выраженным болевым синдромом и инкрустированной формой лучевого цистита.
Результаты лечения больных второй группы представлены в таблице 3. Следует отметить выраженное противовоспалительное действие УРО-ГИАЛА. Так, частота ночного мочеиспускания сократилась в два раза более чем у 56% пациентов с неосложненными циститами и у 59% с осложненными циститами. Лейкоцитурия уменьшилась в два раза у больных с осложненными циститами и практически не выявлялась у пациентов с неосложненными циститами (12%), а бактериурия сохранилась только у 27 и 25% больных в обеих подгруппах соответственно.
Основные УЗИ-признаки воспаления (взвесь в просвете мочевого пузыря и утолщение его стенок) исчезли у подавляющего числа больных. Однако УРО-ГИАЛ практически не оказал действия на инкрустированные циститы, особенно у больных со сниженным объемом мочевого пузыря.
Характеристика цистоскопических признаков лучевых циститов у больных второй группы до и после лечения продемонстрирована в таблице 4. Гиперемия и отек беспокоили менее чем 25% больных как с неосложненной, так и осложненной формой цистита. Частота эрозии у пациентов с неосложненными циститами уменьшилась в четыре раза. Однако более чем у 70% пациентов сохранились телеангиоэктазии. Язва мочевого пузыря у больных с осложненными циститами уменьшилась в размерах и очистилась от фибрина.
Можно сделать вывод, что применяемая схема лечения – инстилляции УРО-ГИАЛА – наиболее эффективна у пациентов с выраженным воспалительным процессом и болевым синдромом, связанным с воспалением стенок мочевого пузыря, и может применяться у больных с любой формой лучевого цистита, осложненного бактериальной инфекцией.
Результаты лечения больных третьей группы представлены в таблице 5. Почти у половины больных с неосложненными и осложненными циститами в два раза уменьшилась частота ночного мочеиспускания. У 75 и 90% пациентов соответственно сохранилась лейкоцитурия. Однако бактериурия почти у половины больных в обеих подгруппах не определялась, а макрогематурия исчезла у всех пациентов.
Сравнительная характеристика УЗИ-признаков лучевых циститов у больных третьей группы продемонстрировала достоверное увеличение объема мочевого пузыря у пациентов с микроцистисом, однако в меньшей степени Рексод оказал положительное действие на инкрустацию стенок мочевого пузыря и наличие взвеси в его просвете.
Что касается выраженности цистоскопических признаков лучевых циститов у больных третьей группы (табл. 6), то в результате лечения язва мочевого пузыря исчезла у всех больных, однако более чем у 60% пациентов с осложненными циститами сохранялись признаки воспаления (гиперемия и отек). Таким образом, Рексод можно рекомендовать больным с геморрагическим синдромом, при язвенном лучевом цистите и сниженном объеме мочевого пузыря.
Заключение
Следует отметить, что используемые препараты (Димексид, УРО-ГИАЛ и Рексод) имеют разную направленность действия. В частности, при выраженном фиброзе стенки мочевого пузыря предпочтение следует отдавать применению инстилляций раствора Димексида. При выраженном воспалительном процессе, сопровождающемся поверхностным нарушением слизистой мочевого пузыря, а также атрофии слизистой наиболее эффективным оказалось применение УРО-ГИАЛА. У больных с гематурией и глубокими нарушениями целостности слизистой мочевого пузыря (язвенно-некротический цистит) наиболее высокие результаты продемонстрировало применение супероксиддисмутазы. Выбор метода лечения должен основываться на данных субъективных жалоб и объективных методов исследования.
Источник
