Гиперурикемия первичная и вторичная подагра
Самым частым нарушением обмена пуринов является повышенное образование мочевой кислоты с развитием гиперурикемии. Особенностью является то, что растворимость солей мочевой кислоты (уратов) в плазме крови невелика и при превышении порога растворимости в плазме (около 0,7 ммоль/л) они кристаллизуются в периферических зонах с пониженной температурой.
В зависимости от длительности и тяжести гиперурикемия проявляется:
- Появление тофусов (греч. tophus – пористый камень, туф) – отложение уратных кристаллов в коже и подкожных слоях, в мелких суставах ног и рук, в сухожилиях, хрящах, костях и мышцах.
- Нефропатии в результате кристаллизации мочевой кислоты с поражением почечных канальцев и мочекаменная болезнь.
- Подагра – поражение мелких суставов.
Для диагностики нарушений используют определение концентрации мочевой кислоты в крови и моче.
Нарушения обмена пуринов
Подагра
Когда гиперурикемия принимает хронический характер, говорят о развитии подагры (греч. poclos – нога, agra – захват, дословно – “нога в капкане”).
В крови мочевая кислота находится в форме ее солей – уратов натрия. Из-за низкой растворимости ураты способны оседать в зонах с пониженной температурой, например, в мелких суставах стоп и пальцев ног. Накапливающиеся в межклеточном веществе ураты некоторое время фагоцитируются, но фагоциты не способны разрушить пуриновое кольцо. В результате это приводит к гибели самих фагоцитов, к выходу лизосомальных ферментов, активации свободнорадикального окисления и развитию острой воспалительной реакции – развивается подагрический артрит. В 50-75% случаев первым признаком заболевания является мучительная ночная боль в больших пальцах ног.
Длительное время подагру считали “болезнью гурманов”, однако затем внимание исследователей переместилось к наследственному изменению активности ферментов метаболизма пуринов:
- увеличение активности ФРДФ-синтетазы – приводит к избыточному синтезу пуринов,
- уменьшение активности гипоксантин-гуанин-фосфорибозил-трансферазы – из-за этого ФРДФ не используется для реутилизации пуриновых оснований, а участвует в первой реакции их синтеза. В результате возрастает количество разрушающихся пуринов и одновременно повышается их образование.
Оба ферментативных нарушения рецессивны и сцеплены с X-хромосомой. Подагрой страдает 0,3-1,7% взрослого населения земного шара, соотношение заболевших мужчин и женщин составляет 20 : 1.
Основы лечения
Диета – снижение поступления предшественников мочевой кислоты с пищей и уменьшение ее образования в организме. Для этого из рациона исключаются продукты, содержащих много пуриновых оснований – пиво, кофе, чай, шоколад, мясные продукты, печень, красное вино. Предпочтение отдается вегетарианской диете с количеством чистой воды не менее 2 л в сутки.

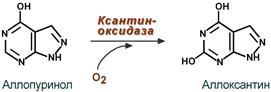
Реакция превращения аллопуринола
К лекарственным средствам лечения подагры относят аллопуринол, по структуре схожий с гипоксантином. Ксантиноксидаза окисляет аллопуринол в аллоксантин, и последний остается прочно связанным с активным центром фермента и ингибирует его. Фермент осуществляет, образно говоря, самоубийственный катализ. Как следствие, ксантин не превращается в мочевую кислоту, и поскольку гипоксантин и ксантин лучше растворимы в воде, то они более легко выводятся из организма с мочой.
Мочекаменная болезнь
Мочекаменная болезнь заключается в образовании солевых кристаллов (камней) разной природы в мочевыводящих путях. Непосредственно образование мочекислых камней составляет около 15% от всех случаев этой болезни. Мочекислые камни в мочевыводящих путях откладываются примерно у половины больных подагрой.
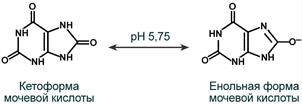
Две переходные формы мочевой кислоты при pH 5,75
Наиболее часто такие камни представлены в дистальных канальцах и собирательных трубочках. Причиной отложения кристаллов мочевой кислоты является гиперурикемия и повышенное выведение уратов натрия с мочой. Главным провоцирующим фактором кристаллизации является увеличение кислотности мочи. При понижении рН мочи ниже 5,75 ураты (енольная форма) переходят в менее растворимую кетоформу и кристаллизуются в почечных канальцах.
Закисление мочи (в норме 5,5-6,5) возникает по различным причинам. Это может быть избыточное питание мясопродуктами, содержащими большое количество нуклеиновых кислот, аминокислот и неорганических кислот, что делает такую пищу “кислой” и снижает рН мочи. Также кислотность мочи усиливается при ацидозах различного происхождения (Кислотно-основное состояние).
Кристаллы в почках могут иметь различную природу: 70-75% больных мочекаменной болезнью имеют камни щавелевой кислоты (оксалаты), 15% – мочевой кислоты, 10% – кальций-фосфатные, карбонатные, цистиновые камни. Самый большой почечный камень был извлечен 29.12.1952 из почки 80-летней женщины в Лондоне. Камень весил 6 кг 294 г.
Основы лечения
Так же, как при подагре, лечение сводится к беспуриновой диете и использованию аллопуринола. В дополнение рекомендуется растительная диета, приводящая к защелачиванию мочи, что увеличивает в моче долю более растворимой в воде енольной формы мочевой кислоты. Вместе с этим, уже имеющиеся кристаллы мочевой кислоты (а также кристаллы оксалатов) способны растворяться при подщелачивании мочи.
Лекарственное лечение непременно должно сопровождаться соблюдением беспуриновой диеты с большим количеством чистой воды, в противном случае неизбежно появление ксантиновых кристаллов в тканях и ксантиновых камней в почках.
Синдром Леша-Нихана
Болезнь Леша-Нихана (частота 1:300000) – это полное врожденное отсутствие активности гипоксантин-гуанин-фосфорибозил-трансферазы, фермента, отвечающего за реутилизацию пуриновых оснований. Признак рецессивный и сцеплен с Х-хромосомой. Впервые его описали в 1964 г в США студент-медик Майкл Леш и педиатр Уильям Нихан.
Дети рождаются клинически нормальными, только к 4-6 месяцу обнаруживаются отклонения в развитии, а именно – отставание физического развития (с трудом держит голову), повышенная возбудимость, рвота, периодическое повышение температуры. Выделение мочевой кислоты можно обнаружить еще раньше по оранжевой окраске пеленок. К концу первого года жизни симптомы нарастают, развивается нарушение координации движений, хореоатетоз, корковый паралич, спазм мышц ног. Наиболее характерный признак заболевания проявляется на 2-3-м году жизни – аутоагрессия или самокалечение – неодолимое стремление детей кусать себе губы, язык, суставы пальцев на руках и ногах. Агрессия больных распространяется также на неживые предметы и окружающих людей. Нарушения интеллекта выражены, его снижение может быть до IQ≈60.
Лечение основано на беспуриновой диете с большим количеством чистой воды и с использованием аллопуринола. Производится контроль деятельности пациента с помощью физических ограничений и психологической терапии.
Источник
Метаболическая гиперурикемия и подагра обусловлены повышенной продукцией мочевой кислоты, о чем можно судить по повышенной экскреции (более 600 мг/сут) мочевой кислоты даже в условиях ограниченного приема пуринов с пищей. На долю этого типа подагры приходится менее 10% всех случаев этого заболевания.
Мочевая кислота, как известно, является конечным продуктом метаболизма пуринов (см. рис. 11). Скорость синтеза мочевой кислоты у человека определяется внутриклеточной концентрацией 5-фосфорибозил-1-пирофосфата (ФРПФ): при повышении уровня ФРПФ в клетке синтез мочевой кислоты усиливается, а при снижении — уменьшается.
Избыточная продукция мочевой кислоты может быть первичной и вторичной. Первичная гиперурикемия обусловлена врожденной недостаточностью гипоксантингуанинфосфорибозил-трансферазы или повышенной активностью ФРПФ-синтетазы и наследуется сцеплено с Х-хромосомой. Вторичная гиперурикемия, обусловленная гиперпродукцией мочевой кислоты, может быть связана со многими причинами:
- • ускорением биосинтеза пуринов de novo;
- • недостаточностью глюкозо-6-фосфатазы (например, при болезни накопления гликогена I типа), при которой отмечается повышенная продукция мочевой кислоты и ускоряется синтез пуринов de novo;
- • ускорением синтеза ФРПФ;
- • ускорением распада пуриновых нуклеотидов.
Последние две причины включаются при дефиците в клетке глюкозы как источника энергии. Полагают, что у большинства больных со вторичной гиперурикемией на почве избыточной продукции мочевой кислоты основное нарушение заключается в ускорении кругооборота нуклеиновых кислот, что характерно для многих заболеваний: мие- лоз, лимфолейкоз, миелома, вторичная полицитемия, пернициозная анемия, талассемия, гемолитические анемии, инфекционный монону- клеоз, карцинома и т. д. Ускорение кругооборота нуклеиновых кислот приводит к гиперурикемии и компенсаторному повышению скорости биосинтеза пуринов de novo.
Почечная гиперурикемия и подагра обусловлены снижением экскреции мочевой кислоты почками. На долю этого типа подагры приходится до 90% всех случаев. Экскреция мочевой кислоты зависит от клубочковой фильтрации, канальцевой реабсорбции и секреции. Уменьшение скорости фильтрации (1-й фактор), усиление реабсорбции в проксимальных канальцах (2-й фактор) или снижение скорости секреции (3-й фактор) мочевой кислоты снижают ее почечную экскрецию. Вполне вероятно, что у больных подагрой имеют место все три фактора.
Почечный тип гиперурикемии и подагры может быть первичным и вторичным. Первичная почечная подагра встречается у больных с патологией почек: поликистоз, свинцовая нефропатия. Вторичная почечная гиперурикемия может наблюдаться при приеме диуретиков, уменьшающих объем циркулирующей плазмы, что сопровождается снижением фильтрации мочевой кислоты, усилением ее канальциевой реабсорбции и уменьшением секреции мочевой кислоты. Ряд других лекарственных средств (аспирин в низких дозах, никотиновая кислота, пиразинамид, этанол) также вызывает гиперурикемию посредством снижения экскреции мочевой кислоты, однако механизмы этого до сих пор не установлены.
Нефрогенный несахарный диабет, недостаточность надпочечников, уменьшая ОЦП, индуцируют гиперурикемию. Гиперурикемия может быть следствием конкурентного ингибирования секреции мочевой кислоты избытком органических кислот, которые секретируются аналогичными механизмами почечных канальцев, что и мочевая кислота. Избыток органических кислот наблюдается при голодании, алкогольном и диабетическом кетоацидозе, лактацидозе любого происхождения.
Гиперурикемия, характерная для гиперпара- и гипопаратиреоза, гипотиреоза, также может иметь почечную основу, но механизм ее возникновения неясен. Эволюция подагры проходит четыре стадии:
- • бессимптомная гиперурикемия;
- • острый подагрический артрит;
- • межкритический период;
- • хронические подагрические отложения в суставах.
Стадия бессимптомной гиперурикемии характеризуется повышением уровня урата в сыворотке крови, но симптомы артрита, подагрические отложения в суставах или мочекислые камни отсутствуют. У мужчин, подверженных классической подагре, гиперурикемия начинается в период полового созревания, а у женщин из группы риска — с наступлением менопаузы. Бессимптомная гиперурикемия может сохраняться в течение всей жизни. Несмотря на то, что гиперурикемия определяется практически у всех больных подагрой, лишь только у 5% лиц с гиперурикемией когда-либо развивается эта болезнь.
Стадия бессимптомной гиперурикемии заканчивается с первым приступом подагрического артрита или нефролитиаза. Артрит, как правило, предшествует нефролитиазу, который развивается обычно через 20—30 лет стойкой гиперурикемии.
Следующая стадия — острый подагрический артрит. Причины, вызывающие начальную кристаллизацию урата натрия в суставе после длительного периода бессимптомной гиперурикемии, изучены неполностью, хотя известно, что отложению уратов в тканях способствует сдвиг pH в кислую сторону и нарушение обмена мукополисахаридов, поддерживающих ураты в растворенном состоянии. Постоянная гипе- рурикемия в конечном итоге приводит к формированию микроотложений в плоских клетках синовиальной оболочки и накоплению урата натрия в хряще на протеогликанах, обладающих высоким сродством к нему.
Различные причины, но чаще всего травмы, сопровождающиеся разрушением микроокружения и ускорением кругооборота протеогли- канов хряща, обусловливают высвобождение кристаллов урата в синовиальную жидкость. Низкая температура в суставе, неадекватная реабсорбции воды и урата из синовиальной жидкости в полости сустава обусловливают накопление в нем достаточного количества кристаллов урата. Кристаллы мочевой кислоты фагоцитируются в суставах нейтрофилами, затем разрушают их с высвобождением лизосомальных ферментов, которые являются медиаторами острого подагрического воспаления. Острый приступ артрита провоцируется рядом моментов, в том числе:
- • фагоцитозом кристаллов лейкоцитами с быстрым высвобождением из них хемотаксических белков;
- • активацией калликреиновой системы;
- • активацией комплемента с последующим образованием хемотаксических его компонентов;
- • разрушением кристаллами уратов лизосом лейкоцитов и выделением в синовиальную жидкость лизосомных продуктов.
Если в понимании патогенеза острого подагрического артрита достигнут определенный прогресс, то многие вопросы, касающиеся спонтанного прекращения острого приступа и эффекта колхицина, еще ждут ответа.
Вначале крайне болезненный артрит затрагивает один из суставов со скудной общей симптоматикой. Позднее в процесс вовлекается несколько суставов на фоне лихорадочного состояния. Продолжительность приступов различна, но все же ограничена. Они перемежаются с бессимптомными периодами. Острый подагрический артрит — это болезнь преимущественно ног. Чем дистальнее место поражения, тем более типичны приступы. Иногда развивается подагрический бурсит, причем чаще всего в процесс вовлекаются сумки коленного и локтевого суставов. Перед первым резким приступом подагры больные могут ощущать постоянную болезненность с обострениями, но чаще первый приступ бывает неожиданным и имеет «взрывной» характер. Он, как правило, начинается в ночное время, боль в воспаленном суставе чрезвычайно сильна.
Приступ может провоцироваться травмой, приемом алкоголя и некоторых лекарственных средств, погрешностями в диете, хирургической операцией. В течение нескольких часов интенсивность достигает пика, отчетливо проявляются признаки прогрессирующего воспаления, нарастает лейкоцитоз, повышается температуру тела, увеличивается СОЭ.
Приступы подагры могут продолжаться в течение одного или двух дней или нескольких недель, но они купируются, как правило, спонтанно. Последствий не остается, и выздоровление кажется полным, т. е. наступает 3-я стадия — бессимптомная фаза, называемая межкритическим периодом, в течение которого больной не предъявляет никаких жалоб. У 7% больных второго приступа вообще не наступает, а у 60% — болезнь рецидивирует в течение года. Однако межкритический период может длиться даже до 10 лет и завершаться повторными приступами, каждый из которых становится все более длительным, а ремиссии все менее полными. При последующих приступах в процесс вовлекается обычно несколько суставов, сами приступы становятся более тяжелыми, более продолжительными и сопровождаются лихорадкой.
У нелеченных больных скорость продукции урата превышает скорость его элиминации. В итоге в хрящах, синовиальных оболочках, сухожилиях и мягких тканях появляются скопления кристаллов урата натрия. Подагрические отложения часто локализуются вдоль локтевой поверхности предплечья в виде выпячиваний сумки локтевого сустава, по ходу ахиллова сухожилия, в области завитка и противоза- витка ушной раковины. Они могут изъязвляться и выделять беловатую вязкую жидкость, богатую кристаллами урата натрия. Подагрические отложения редко инфицируются.
У 90% больных с подагрическим артритом выявляется различная степень нарушения функции почек — нефропатия. До введения в практику гемодиализа 17—25% больных подагрой умирали от почечной недостаточности.
Различают несколько типов повреждения почечной паренхимы:
- • уратная нефропатия, обусловленная отложением кристаллов урата натрия в интерстициальную ткань почек;
- • обструктивная нефропатия, обусловленная образованием кристаллов мочевой кислоты в собирательных канальцах, почечной лоханке или мочеточниках.
Факторы, способствующие образованию отложений урата в почках, неизвестны. Нефролитиаз встречается с частотой 1—2 случая на 1000 больных подагрой. Ведущим фактором, способствующим образованию мочекислых камней, служит повышенная экскреция мочевой кислоты. Гиперурикацидурия может быть результатом первичной подагры, врожденного нарушения метаболизма пуринов, приводящего к повышению продукции мочевой кислоты, миелопролиферативного заболевания и других неопластических процессов. Если экскреция мочевой кислоты с мочой превышает 1100 мг/сут., частота камнеобразования достигает 50%.
Образование мочекислых камней коррелирует также с гиперурике- мией: при уровне мочевой кислоты 130 мг/л и выше частота камнеобразования достигает примерно 50%. Образованию мочекислых камней способствует чрезмерное закисление мочи; концентрированность мочи. Кристаллы мочевой кислоты могут служить ядром для образования кальциевых камней.
Принципы патогенетической профилактики и лечения больных с нарушением пуринового обмена. Поскольку острый подагрический артрит — это воспалительный процесс, то следует проводить противовоспалительное лечение, прежде всего колхицином, который стабилизирует мембраны лизосом, подавляет хемотаксис и фагоцитоз, оказывает антимитотическое действие на нейтрофилы, до наступления облегчения состояния больного или появления побочных реакций со стороны желудочно-кишечного тракта. При внутривенном введении колхицина побочные эффекты со стороны желудочно-кишечного тракта не возникают.
К числу побочных эффектов приема колхицина относятся: угнетение функции костного мозга, аллопеция, недостаточность печени, психическая депрессия, судороги, восходящий паралич, угнетение дыхания. Из других противовоспалительных средств эффективны индометацин, фенилбутазон, напроксен, фенопрофен. Препараты, стимулирующие экскрецию мочевой кислоты, и аллопуринол при остром приступе подагры неэффективны.
При неэффективности или противопоказаниях к колхицину и нестероидным противовоспалительным средствам прибегают к системному (внутривенно или перорально) или местному (в сустав) введению глюкокортикоидов. Это лечение особенно целесообразно при невозможности использовать стандартную лекарственную схему.
Дефицит этого фермента уменьшает расход фосфорибозилпирофосфата, который накапливается в больших, чем в норме, концентрациях, ускоряя биосинтез пуринов de novo, что обусловливает гиперпродукцию мочевой кислоты. Успешно поддается воздействию аллопуринола — ингибитора ксантиноксидазы, которая катализирует превращение ксантина и гипоксантина в мочевую кислоту.
Для уменьшения вероятности рецидива острого приступа рекомендуется:
- • ежедневный профилактический прием колхицина или индомета- цина;
- • контролируемое уменьшение массы тела у больных с ожирением;
- • устранение ряда провоцирующих факторов (алкоголь);
- • применение антигиперурикемических препаратов с целью поддержания уровня урата в сыворотке крови ниже 70 мг/л, т. е. в той минимальной концентрации, при которой урат насыщает внеклеточную жидкость. Урикозурические препараты (пробенецид, сульфинпи- разон) повышают почечную экскрецию уратов;
- • ограничение потребления продуктов, богатых пуринами: мяса, рыбы, печени, бобов.
Гиперурикемию можно корригировать с помощью аллопуринола, ингибирующего ксантиноксидазу, и тем самым уменьшать синтез мочевой кислоты. С целью профилактики мочекислой нефропатии прибегают к водным нагрузкам и диуретикам, ощелачиванию (гидрокарбонат натрия) мочи, чтобы мочевая кислота превращалась в растворимый урат натрия, назначению аллопуринола.
Источник
